САХАРОЗАМЕНИТЕЛИ
Классификация сахарозаменителей
Поиск заменителей сахара, активно проводимый в настоящее время во многих странах, обусловлен в значительной степени необходимостью оптимизации питания здоровых людей, а также возможностью решения вопросов рационального питания людей, страдающих определенными заболеваниями. С незапамятных времен известно, что причиной развития целого ряда болезней становится неправильный образ жизни и, в частности, привычки питания. В настоящее время эти заключения получили научное подтверждение, особенно относительно злоупотребления сладкой и жирной пищей. Предлагая древнему человеку сладкие плоды, природа использовала сладкий вкус как приманку. Стремясь насладиться вкусом пищи, наш первобытный предок "заодно" потреблял витамины, микроэлементы, клетчатку — все, что чрезвычайно нужно организму. Однако человек научился выделять и употреблять сладкое в отдельности от других полезных ингредиентов. Привыкнув к сладкому с детства, люди с годами увеличивают свои потребности, не учитывая, что их организм не рассчитан на переработку такого количества сладких веществ. Поэтому, прежде чем начинать лечение наших пациентов, мы рекомендуем: "Если заболел и хочешь быть здоров — измени образ жизни". Существует выражение, высказанное американскими диабетологами: "Легче изменить религию человека, чем привычки питаться". Действительно, постоянно употребляя сладкую, жирную, соленую, острую пищу, не каждый человек имеет силу воли отказаться от привычек, которые складывались годами. Необходимость исключать или резко ограничить употребление сахара в питании создает у людей состояние дискомфорта. Особенно трудно переносят исключение сладостей дети и подростки. Стремление сохранить привычные вкусовые свойства пищи привело к необходимости разработать способы "обмана" вкусовых ощущении человека, когда, воспринимая привычный и приятный вкус, люди не наносят вред своему организму, как при употреблении избыточного количества вредных ингредиентов. В настоящее время предпринимаются попытки создания солезаменителей, жирозаменителей и сахарозаменителей. Учитывая негативные последствия, наступающие от неумеренного потребления Сахаров, особое внимание уделялось созданию сахарозаменителей, которые можно было бы употреблять, удовлетворяя вкусовые чувства и не вызывая негативных последствий. Поэтому к саха-розаменителям предъявляются следующие требования:
1. Приятный сладкий вкус.
2. Безвредность.
3. Отсутствие влияния на углеводный обмен.
4. Хорошая растворимость в воде.
5. Стойкость к кулинарной обработке (температуре).
В последние десятилетия в экономически развитых странах ведется поиск и создаются производства новых, безвредных для человека, низкокалорийных подслащивающих веществ, способных удовлетворять потребности организма больных сахарным диабетом и лиц с избыточной массой тела (Я.Л. Герма-нюк, 1986, 1987; Г.А. Дунаевский и соавт., 1987). Потребляя эти продукты, можно четко регулировать поступление калорий и не чувствовать себя ущемленным в сладости. Необходимо отметить, что применение сахарозаменителей не является необходимостью с физиологической точки зрения. Их использование диктуется психологией человека, традициями и привычками употребления сладкой пищи.
Многие заменители сахара различаются между собой по химическому составу, способам получения, долей участия в обмене веществ, их переносимостью. Одним из основных показателей качества сахарозаменителей является интенсивность сладости. В настоящее время известно много подобных веществ, обладающих сладким вкусом, что требует их классификации по различным признакам. Реальное число практически используемых сладких веществ не так велико, поскольку большинство из них обладают либо слабовыраженным сладким вкусом, либо проявляют токсичность или нежелательные побочные эффекты.
Один из принципов классификации подсластителей — разделение их по степени сладости относительно сахарозы. Те подсластители, уровень сладости которых близок к сахарозе, называют объемными подсластителями, а вещества, во много раз слаще сахарозы — интенсивными подсластителями (B.J. Rolls, 1991; A. Drenowski, 1995).
 Некоторые объемные подсластители для своего растворения требуют дополнительного количества теплоты, вследствие чего раствор охлаждается, а во рту возникает чувство "холодка". Эти свойства, в разной степени, выражены у ксилита, сорбита и маннита. Поэтому их часто используют как увлажнители, для снижения карамелизации, для охлаждения ротовой полости в безалкогольных напитках. В некоторых видах мороженого объемные подсластители могут заменить сахарозу, благодаря их технологическим преимуществам — предотвращать образование зернистой структуры вследствие кристаллизации при низких температурах.
Некоторые объемные подсластители для своего растворения требуют дополнительного количества теплоты, вследствие чего раствор охлаждается, а во рту возникает чувство "холодка". Эти свойства, в разной степени, выражены у ксилита, сорбита и маннита. Поэтому их часто используют как увлажнители, для снижения карамелизации, для охлаждения ротовой полости в безалкогольных напитках. В некоторых видах мороженого объемные подсластители могут заменить сахарозу, благодаря их технологическим преимуществам — предотвращать образование зернистой структуры вследствие кристаллизации при низких температурах.
 Важной с практической точки зрения является классификация подсластителей по калорийности. При этом различают калорийные подсластители, прием которых необходимо учитывать в диетах, направленных на снижение массы тела, и их возможное влияние на уровень глюкозы крови, а также бескалорийные, не имеющие противопоказаний.
Важной с практической точки зрения является классификация подсластителей по калорийности. При этом различают калорийные подсластители, прием которых необходимо учитывать в диетах, направленных на снижение массы тела, и их возможное влияние на уровень глюкозы крови, а также бескалорийные, не имеющие противопоказаний.
Калорийные вещества со сладким вкусом называют также сахарозаменителями. Имея энергетическую ценность, близкую к сахарозе, они метаболизируются в организме более плавно, чем сахар, с меньшей потребностью в инсулине, а при умеренном потреблении не приводят к выраженной гипергликемии. Например, такие сахарозаменители: ксилит, сорбит, фруктоза. Бескалорийные вещества еще называют собственно подсластителями. Они не обладают или почти не обладают энергетической ценностью, поэтому их метаболизм не зависит от инсулина и не влияет на уровень глюкозы в крови. Однако на практике принято употреблять термины "калорийные" и "бескалорийные" сахарозаменители.
Все известные сладкие вещества можно также разделить на две большие группы: природные и синтетические. К числу природных сладких веществ относятся моносахариды и олиго-сахариды, гидролизаты крахмала, сахаридные спирты и сладкие вещества несахаридного типа, а также подсластители растительного происхождения.
Синтетические подслащивающие вещества, вследствие полного отсутствия у них калорийности, стали вытеснять природные "калорийные" сладкие вещества из некоторых пищевых продуктов и из рациона питания диабетиков. В отличие от известных сладких углеводов, синтетические подслащивающие вещества универсально удовлетворяют требованиям диеты. При наличии сладкого вкуса эти вещества имеют совершенно отличный от углеводов путь обмена. Однако ряд авторов указывают и на отрицательные свойства синтетических подсластителей. Так, сахароза вызывает ощущение сладкого без дополнительного привкуса в широком интервале концентраций (от менее 0,5 % до более чем 100 %), в то время как у некоторых синтетических сахарозаменителей наблюдается переход от сладкого вкуса к иному при незначительных изменениях концентрации. Поэтому их рекомендуют применять в определенном диапазоне доз. Кроме того, сахароза, в отличие от синтетических сахарозаменителей, обладает консервирующими свойствами, что влияет на сохраняемость продуктов.
Каждое из известных на данный момент веществ-сахароза-менителей имеет свои преимущества и недостатки. Поэтому рекомендуют смешивать малые дозы сразу нескольких таких веществ. Такие смеси придают сладкий вкус в результате суммарного действия более низких доз отдельных ингредиентов, чем каждого в отдельности. При снижении количества каждого из компонентов нежелательный эффект уменьшается или стирается вовсе. В состав смесей иногда входят ограниченные количества натуральных простых Сахаров, таких, как фруктоза, сорбит или ксилит, а также синтетические заменители, такие, как ацесульфам "К" или аспартам. Можно принять за основу совет использовать для смеси по меньшей мере два вещества. Кроме сахарозаменителей и подсластителей отдельно выделяют также группу веществ — модификаторов вкуса, изменяющихся вкусовые восприятия. Говоря о сахарозаменителях, необходимо отметить, что они относятся не к пищевым продуктам, а к пищевым добавкам. Поэтому целесообразно рассмотреть особенности этих веществ, употребляемых человеком с пищей.
Очень важным моментом для широкого внедрения сахароза-менителей является их безвредность. Для проверки безопасности применения сахарозаменителей и определения средней  дозы потребления (Average Daily Intake) необходимо определить возможный 100-кратный экспериментальный уровень в режиме питания. Согласно рекомендациям Европейского комитета по продуктам питания, не имеет смысла устанавливать этот показатель для мальтола и подсластителей на его основе (так называемых гидрогенизированных сиропов глюкозы), а для синтетических сахарозаменителей такие исследования обязательны.
дозы потребления (Average Daily Intake) необходимо определить возможный 100-кратный экспериментальный уровень в режиме питания. Согласно рекомендациям Европейского комитета по продуктам питания, не имеет смысла устанавливать этот показатель для мальтола и подсластителей на его основе (так называемых гидрогенизированных сиропов глюкозы), а для синтетических сахарозаменителей такие исследования обязательны.
Каждое из известных на данный момент веществ-сахароза-менителей имеет свои преимущества и недостатки. Поэтому рекомендуют смешивать малые дозы сразу нескольких таких веществ. Такие смеси придают сладкий вкус в результате суммарного действия более низких доз отдельных ингредиентов, чем каждого в отдельности. При снижении количества каждого из компонентов нежелательный эффект уменьшается или стирается вовсе. В состав смесей иногда входят ограниченные количества натуральных простых Сахаров, таких, как фруктоза, сорбит или ксилит, а также синтетические заменители, такие, как ацесульфам "К" или аспартам. Можно принять за основу совет использовать для смеси по меньшей мере два вещества. Кроме сахарозаменителей и подсластителей отдельно выделяют также группу веществ — модификаторов вкуса, изменяющихся вкусовые восприятия. Говоря о сахарозаменителях, необходимо отметить, что они относятся не к пищевым продуктам, а к пищевым добавкам. Поэтому целесообразно рассмотреть особенности этих веществ, употребляемых человеком с пищей.
Еще с доисторических времен люди обнаружили, что существуют определенные вещества, после добавления которых к пище ее вкусовые качества значительно улучшаются. Под термином "пищевые добавки" подразумевают природные или синтетические вещества, которые не имеют пищевой или биологической ценности, а специально вводятся в пищу для придания ей определенных свойств. Они могут придавать продуктам стойкость, органические, технологические свойства и, чаще всего, не применяются самостоятельно (IJL Козярин, 2000).
Все пищевые добавки принято условно подразделять на следующие группы.
• Красители (самостоятельно или в смеси).
• Консерванты (разрешается комбинация не более двух
консервантов).
• Регуляторы кислотности.
• Антиоксиданты.
• Эмульгаторы.
Сладкие вещества растительного происхождения
Солодка голая
Значительную группу природных сахарозаменителей составляют вещества растительного происхождения, среди которых наиболее известна с древнейших времен солодка голая (сладкое дерево, лакрица), Glycyrrhiza glabra. Это многолетнее травянистое растение, семейства бобовых, имеет народное название лакричник сладкий или солодовый корень. Его использование насчитывает несколько тысяч лет. Еще в клинописных табличках древнего Вавилона имеется упоминание о применении растертого корня "сладкого дерева" с маслом и пивом для лечения кашля. Росла она в саду Вавилонского царя Мардука-палиддина И. Описание этого растения встречается в египетских папирусах. Особенно большим почетом она пользовалась в китайской медицине. Сведения о солодке были записаны в книге "Бень-цао" ("Книга о травах"), которая появилась с изобретением письменности в Китае. Сами же сведения о пользе солодки были собраны "отцом медицины" Китая полулегендарным князем Шеньнунем (почти 3 тыс. лет до н.э.). В старых рецептах китайской медицины говорилось, что солодка облегчает боль, усиливает кровообращение, улучшает работу желудка, селезенки и легких, лечит лихорадку. По мнению китайских врачей, корень солодки омолаживает организм. Поэтому они ценили его так же, как женьшень, и старались добавить во все лекарства, считая, что он усиливает эффект других лекарственных средств.
 Применялась солодка и в тибетской медицине. Показательно, что в состав 40 из 150 рецептов тибетской медицины входит солодка. По частоте использования и по популярности она превосходила женьшень. В медицинском руководстве "Худ-ши" говорится, что солодка "придает цветущий вид", "упитывает" и "способствует долголетию". Очень широко она применялась у скифов Причерноморья, которые продавали корень в европейские страны, где он получил название "скифский корень". Известный греческий врач Диоскорид (I в. н.э.) назвал "скифский корень" за его сладкий вкус глицирризой, а римляне переделали это название в более созвучное их языку слово "ликвирица", отсюда возникло еще одно название сладкого корня — лакричный корень. Знали о свойствах солодки Гиппократ, Гален и Авиценна. Она упоминается во всех травниках и во всех фармакопеях мира.
Применялась солодка и в тибетской медицине. Показательно, что в состав 40 из 150 рецептов тибетской медицины входит солодка. По частоте использования и по популярности она превосходила женьшень. В медицинском руководстве "Худ-ши" говорится, что солодка "придает цветущий вид", "упитывает" и "способствует долголетию". Очень широко она применялась у скифов Причерноморья, которые продавали корень в европейские страны, где он получил название "скифский корень". Известный греческий врач Диоскорид (I в. н.э.) назвал "скифский корень" за его сладкий вкус глицирризой, а римляне переделали это название в более созвучное их языку слово "ликвирица", отсюда возникло еще одно название сладкого корня — лакричный корень. Знали о свойствах солодки Гиппократ, Гален и Авиценна. Она упоминается во всех травниках и во всех фармакопеях мира.
Распространена солодка в Южной Европе, Средней Азии, Средиземноморье, на севере Индии, в Афганистане и на Кавказе. Всего насчитывается около 20 видов этого растения. Наиболее известны, кроме солодки голой, также солодка уральская, распространенная в южных районах Сибири и Средней Азии.
Солодка оказывает выраженное отхаркивающее и противовоспалительное действие при заболеваниях верхних дыхательных путей, острых и хронических бронхитах, пневмониях, бронхиальной астме, в том числе в педиатрической практике. Важно, что она хорошо воспринимается и переносится детьми (О.Е. Алешинская и соавт., 1964; С.С. Никитина, 1966).
Препараты корня солодки при приеме внутрь защищают слизистую оболочку желудка и способствуют быстрому заживляющему эффекту в случаях гиперацидного гастрита, язвенной болезни желудка и двенадцатиперстной кишки. Учитывая спазмолитическое и мочегонное действие, солодка полезна при заболеваниях сердца и сосудов. Применяют ее также как легкое слабительное при хроническом запоре.
Полезные свойства солодки были подробно описаны в Са-лернском кодексе здоровья Од о из Мена: "Истинно ведь говорится, что много имеет солодка свойств: ее жар невелик и сладка, и влажна она также; горлу поможет того, кто от кашля страдает, и лечит грудь, и глубины у легких, согрев, исцеляет солодка. Жажду целит и все то, что желудку вредит, изгоняет".
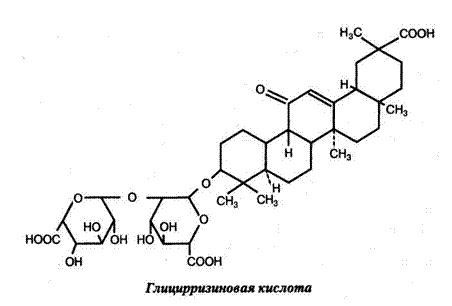
Лечебные свойства препаратов солодки определяются химическими веществами, входящими в ее состав, главное из которых — глицирризин (калиевая или натриевая соль глицир-ризиновой кислоты).
Это соединение из группы сапонинов — высокомолекулярных, безазотистых, гликозидоподобных веществ. Молекула сапонина состоит из сахара и несахарной части — агликона, или сапогенина. Сапонины солодки, раздражая слизистые оболочки, повышают секреторную деятельность желез, оказывают легкое слабительное, отхаркивающее и мочегонное действие (Э.Г. Степанова, 1966).
При гидролизе глицирризин расщепляется на глицирретиновую кислоту, имеющую стероидную структуру и проявляющую свойства кортикостероидов, и две молекулы глюкуроно-вой кислоты. Известно, что глюкуроновые кислоты принимают активное участие при обезвреживании токсических продуктов в печени. Вот почему препараты солодки в старые времена часто использовали при отравлении грибами и других интоксикациях. Учитывая, что стероидная часть молекулы глицир-ризина близка к кортикостероидам (гормонам коры надпочеч-никовых желез), одна из ее солей, названная глицирамом, была предложена в качестве фармакологического препарата для лечения астмы и других болезней, при которых показаны кор-тикостероидные гормоны. Обнаружена способность глицирри-зиновой кислоты и продукта ее гидролиза глицирретиновой кислоты, подобно кортикостероидам, задерживать в организме ионы натрия и повышать выделение калия. Однако свойство препаратов солодки голой проявлять эффекты гормонов коры надпочечников (дезоксикортикостерона) в клинической практике не используется. Корни растения содержат также флавоновые гликозиды: ликвиритин, ликвиритозид, ликвиритигенин (4,7-диоксифла-вон) и глюкозу. Содержится также цирризиновая горечь — до 8,1 %, ликвиритовая кислота, немного эфирного масла, от 11 до 30 мг аскорбиновой кислоты, желтый пигмент и аспарагин. Флавоноиды солодки обладают противовоспалительными свойствами, что позволило сотрудникам Харьковского научно-исследовательского химико-фармацевтического института на их основе разработать препараты "ликвиритон" и "флакарбин" для лечения язвы желудка и двенадцатиперстной кишки.
В медицинской практике использовали следующие препараты солодки: "сироп солодкового корня", "экстракт солодкового корня густой", "экстракт солодкового корня сухой", "сложный порошок солодкового корня" (20 частей порошка корня солодки, 20 частей порошка из листьев сенны, 10 частей порошка плодов укропа, 10 частей серы очищенной и 40 частей сахара в порошке), эликсир грудной (экстракт солодкового корня 60 частей, анисового масла 1 часть, спирта 49 частей, раствора аммиака 10 частей, воды 180 частей).
Многочисленные названия солодки, как народные, так и научные, подчеркивают характернейший признак: сладость ее корня. Эту сладость придают ей многие вещества. Главное из них — глицирризин. Кроме того, приторную сладость корней солодки дополняют глюкоза (до 3 %) и сахароза (около 5 %). Слегка раздражающий, "царапающий" привкус обусловлен содержанием сапонинов. Известно, что водные растворы сапонинов при встряхивании дают пену. В пищевой промышленности это свойство солодки используют для приготовления шипучих напитков, пива, кваса, для лучшего сбивания яичных белков.
Глицирризин используют вместо сахара для подслащивания продуктов, предназначенных для диабетиков — например, в Японии, где запрещено применение сахарина. По интенсивности сладкого вкуса глицирризин в 50-100 раз превосходит сахарозу. Экстракты и сиропы из солодки добавляют в шоколад, карамель и пастилу, мелко нарезанные корни кладут в бочки при квашении капусты, солении огурцов и мочении яблок, а порошок из листьев и корней добавляют в некоторые сорта табака для улучшения его аромата. Глицирризин представляет собой бесцветное кристаллическое вещество, практически нерастворимое в холодной воде, но хорошо растворимое в горячей воде и этаноле. Наиболее выгодно на практике использовать аммонийную и другие соли глицирризиновой кислоты, которые применяются в качестве подсластителей и ароматизаторов для усиления вкусо-ароматических характеристик халвы, безалкогольных напитков, ликеров, пива, мучных кондитерских изделий, мороженого, молочных и других продуктов. Разработаны технологии получения лакричных конфет, с добавкой экстракта корня солодки. Одним из ограничений широкого распространения подсластителей на основе солодки голой является отсутствие сырьевой базы. До сих пор главным источником сбора солодки были природные заросли. Но они за последние 10-15 лет уменьшились в пять с лишним раз. Солодка даже попала в Красную книгу флоры СССР. Поэтому очень остро стоит вопрос о создании культурных плантаций солодки.
Большую работу в этом направлении проделали сотрудники Донецкого ботанического сада АН Украины, доказав, что имеется реальная возможность культивирования солодки голой на больших площадях засоленных, песчаных, смытых, склоновых и других земель, практически не пригодных для выращивания традиционных сельскохозяйственных культур. В образцах корня солодки, выкопанных на юге Донецкой области, содержание глицирризиновой кислоты достигало 15-17 %, что соответствует лучшим образцам из Средней Азии.
Огромный вклад в решение вопроса использования солодки голой внесли труды доктора технических наук В.В. Яременко, разработавшего технологические условия безотходной переработки корня солодки, которые дают возможность получить наряду с лекарственными препаратами ценные сахарозаменители. Подсчитано, что из 1 т корня солодки можно получить 160-200 кг подсластителя (заменителя сахара) с сахарозным эквивалентом 50; 10-25 кг флавоноидной фракции (лекарственного препарата антиоксиданта); 20-40 кг липидной фракции (лекарственного препарата) и 100-200 кг ценной кормовой добавки, содержащей белок, до 25 % крахмала и 30 % клетчатки. Однако следует отметить, что одним из ограничений для более широкого распространения глицирризина и подсластителей на основе солодки является их специфический привкус и аромат. Кроме того, учитывая, что он является аналогом кортикостероидов и проявляет их свойства, его не рекомендуют применять без соответствующих показаний. Поэтому, прежде чем использовать эти вещества в быту и пищевой промышленности, необходимо провести тщательные экспериментальные исследования по их влиянию на эндокринную систему и разработать регламентирующие условия их применения.
Стевия медовая
Среди растений, продуцирующих сладкие вещества, значительный интерес представляет двулистник сладкий (Stevia rebaudiana Bertoni) — растение семейства сложноцветных. Его родина — Южная Америка, Парагвай. Впервые стевию обнаружили испанские конкистадоры в XVI в. вблизи деревни Рио Монде на северо-востоке Парагвая. Затем о ней надолго забыли. Интерес к этому растению возродился после появления в конце XVIII и начале XIX в. ряда статей парагвайского ботаника Moises Bertoni о "медовом листе" (М. Bertoni, 1905, 1911). "Когда впервые смотришь на растение, ничто не привлекает особого внимания, но если кладешь маленький листочек в рот, поражаешься его сладости. Достаточно небольшого фрагмента листа, чтобы ощущать чувство сладости во рту на протяжении часа". Эти слова, написанные в 1899 г. М. Bertoni, открыли и представили миру уникальное растение стевию, или "медовый лист", названное в честь автора Stevia rebaudiana Bertoni.
Это травянистое растение имеет высоту 30-40 см и растет в болотистой местности на бескислотных и гумусных почвах. Его листья в течение столетий использовались жителями местных племен Гуарана и Гаучо, которые называли его Каа-хи ("сладкая трава") и добавляли для подслащивания горьких лекарственных средств и чаев (D. Kinghorn, D. Soejarto, 1991). В настоящее время в городе Баригуи растение настолько популярно, что чай из него продается почти во всех барах и ресторанах, а взбитое молоко, соки и кофе подслащиваются стевией.
Другое народное применение стевии (в Латинской Америке и на Востоке) — для восстановления сил после нервного и физического истощения, для улучшения пищеварения и функции желудочно-кишечного тракта, печени, почек и поджелудочной железы. Применялась она также наружно.
Stevia rebaudiana Bertoni — одна из членов рода Stevia, семейства Compositae. Она приходится родственницей подсолнечнику, ноготкам и т.п. Цветки небольшие, белые, с бледно-пурпурной сердцевиной. Цветочная пыльца может быть очень аллергенной. Стевия способна к самоопылению, и возможно, опыляется насекомыми. Семена маленькие и разносятся ветром через волосяной хохолок. Так как сложноцветные находятся в периоде филогенетической молодости, у них продолжается процесс видообразования, а существующие виды очень изменчивы, они довольно хорошо адаптируются к условиям внешней среды. В настоящее время стевию культивируют за пределами Парагвая — в Японии, Китае, Корее, США, Бразилии и Украине.
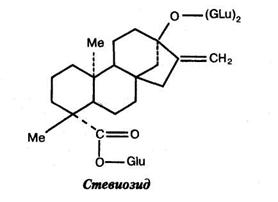 Комплекс сладких веществ стевии состоит из восьми компонентов, различающихся между собой как по степени сладости, так и по количественному содержанию в листьях. По химическому строению сладкие вещества стевии являются тетра-циклическими дитерпеновыми гликозидами, агликоном которых является стевиол, не имеющий вкуса. Ферментативный гидролиз стевиозида приводит к образованию 3 молей D-гдюкозы и 1 моля безвкусного агликона стевиола. При кислотном гидролизе стевиозида образуются D-глюкоза и агликон изостевиол. Структура стевиола подобна таковой стероидных гормонов и обладает слабой антиандрогенной активностью
Комплекс сладких веществ стевии состоит из восьми компонентов, различающихся между собой как по степени сладости, так и по количественному содержанию в листьях. По химическому строению сладкие вещества стевии являются тетра-циклическими дитерпеновыми гликозидами, агликоном которых является стевиол, не имеющий вкуса. Ферментативный гидролиз стевиозида приводит к образованию 3 молей D-гдюкозы и 1 моля безвкусного агликона стевиола. При кислотном гидролизе стевиозида образуются D-глюкоза и агликон изостевиол. Структура стевиола подобна таковой стероидных гормонов и обладает слабой антиандрогенной активностью
(P. Mazzei и соавт., 1968). Стевиозид представляет собой белый кристаллический гигроскопический порошок с температурой плавления 196-198 °С, легко растворимый в воде, устойчив к высокой температуре, поэтому может быть использован для приготовления диетических и консервированных продуктов. Он в 300 раз слаще, чем 0,4 % раствор сахарозы, в 150 — чем 4 % раствор и в 100 раз превышает сладость 10 % раствора сахарозы (М. Bridel, R. Lavielle, 1931; В. Crammer, P. Jkan, 1986; E. Mosetting и соавт., 1963; Jr. Wood и соавт., 1955). Послевкусие сладкого у стевиозида понижается в присутствии сахарозы, фруктозы и глюкозы.
Кроме стевиозида, листья стевии содержат и другие сладкие гликозиды — ребаудиозиды (А, В, С, Д и Е), дулиобиозид и стевиолбиозид с различной степенью сладости (от 50 до 450) по отношению к сахарозе. Наиболее сладким из них является ребаудиозид А (степень сладости 350-450). В сухих листьях стевии содержится около 3 % ребаудиозида. В отличие от стевиозида он более растворим в воде, а неприятное послевкусие его менее интенсивно, чем у стевиозида.
Биосинтез дитерпеновых гликозидов в листьях стевии на начальных этапах имеет общие пути с биосинтезом важного растительного гормона, ускоряющего рост стеблей, прерывающего покой у семян и индуцирующего цветение, — гибберелиновой кислоты. Значение дитерпеновых гликозидов для стевии ещё не установлено. Некоторые учёные считают, что эти вещества отгоняют насекомых, другие предполагают, что они контролируют уровень гибберелиновой кислоты. Установлено, что верхние, более молодые, листья имеют меньшую сладость, чем старые, нижние.
Наиболее широкое распространение в качестве сахарозаменителя получил стевиозид, так как его содержание в растении более высокое. Технология выделения стевиозида из листьев пока довольно сложная. Были попытки синтезировать это соединение, получены некоторые аналоги, обладающие сладким вкусом, но подробных сообщений на эту тему нет. Большой интерес к стевиозиду был проявлен в Японии, где первые растения были интродуцированы в 1970 г., а к 1978 г. продажей продукции, экстрагируемой из листьев, уже занималось 12 компаний. С 1984 г. все ведущие предприятия Японии по производству безалкогольных напитков начали применять стевиозид как полноценный заменитель сахара. В Японии выпускается несколько подсластителей, в состав которых входит стевия: "стевиозин" — практически чистый стевиозид и "стевикс" — смесь сладких гликозидов из листьев стевии. Стевикс обладает более приятным вкусом благодаря ребаудиозиду А, однако он менее сладкий, так как содержит другие менее сладкие гликозиды стевии. Кроме того, смесь стевиозида и глицирризина (экстракт корня солодки) применяется в Японии как подсластитель под названием "Марулерон А". По мнению специалистов Японии, стевиозид перспективен в качестве сахарозаменителя и в экономическом плане — он втрое дешевле сахара (М. Yabu и соавт., 1977).
Очень важным является тот факт, что во многочисленных исследованиях была продемонстрирована низкая токсичность и безопасность стевиозида. В организме стевиозид и ребаудио-зид А метаболизируются в стевиол, который выводится из организма. Наиболее ранние работы, подтверждающие безопасность стевиозида, проведены Ребауди в 1900 г. В 1915 г. Ко-бер, а в 1935 г. Помарет и Лавиелли подтвердили эти результаты. В исследованиях 1975 г. Н. Akashi и Y. Yokoyama сообщили, что ЛД50 для стевиозида составляет 15 г/кг при пероральном введении, а в 1976 г. Митсухаши установил, что ЛД50 при подкожном введении равняется 8,2 г/кг (ЛД50 является дозой, когда гибнет 50 % лабораторных животных). В 1982 г. Кураха-ши с соавторами подтвердили эти данные (Н. Fujita, T. Edahiro, 1979; М. Alvarez, 1986).
Согласно данным Отдела сельского хозяйства США, в 1985 г. потребление сахара на одного человека составило 130 фунтов (1 фунт равен приблизительно 400 г), что равно 2,5 г/кг массы в день. Учитывая, что ЛД50 стевиозида, как указывалось, составляет 15 г/кг, а также то, что он в 300 раз слаще сахара, можно рассчитывать, что этот показатель токсичности будет примерно в 1800 раз меньше, чем то количество сладкого, которое в среднем потребляется человеком в сутки и безопасно для его здоровья. Более 1 тыс. т экстракта стевии ежегодно потребляется в Японии без единого сообщения о токсичности.
Комплексные медико-биологические научные исследования, проведенные сотрудниками ВНИИ химии и технологии лекарственных средств, НИИ гигиены питания МЗ Украины подтвердили данные мировой научной литературы о том, что гликозиды стевии не обладают токсическими, мутагенными, канцерогенными свойствами, не оказывают влияния на репродуктивную функцию (гонадотропное, эмбриотоксическое и тератогенное действие отсутствует) (В.И. Смоляр и соавт., 1992,1993).
Большое количество исследований было проведено при использовании стевии с терапевтической целью. В нескольких предварительных исследованиях в Парагвае и Бразилии установлено гипогликемическое действие травы. Ученые установили, что стевия не оказывает сахароснижающего действия у людей, не больных диабетом (R. Curi и соавт., 1986). Это адаптогенное действие обусловливает безопасность применения растения. При изучении гипогликемизирующего эффекта водного экстракта из листьев стевии (100 г листьев и 1500 мл воды), вводимого перорально животным с аллоксановым диабетом, был обнаружен дозозависимый эффект. Добавление в рацион крыс, содержащий большое количество углеводов, 0,1 % раствора стевиозида приводило к снижению уровня гликогена в печени, но не оказывало влияния на уровень глюкозы в крови (R. Oliveira-Filho и соавт., 1986; Н. Akashi и соавт., 1977). Когда экспериментальным животным давали пищу с высоким содержанием жиров с добавлением 0,1 % раствора стевиозида, у них не выявили изменений тех показателей, которые наблюдались у животных, не получавших стевиозид. Добавление в рацион с высоким содержанием углеводов 10 % порошка из листьев стевии (что соответствует 0,5 % стевиозида в рационе) вызывало значительное снижение уровня глюкозы в крови и гликогена в печени в течение 4 нед введения (A. Viana, J. Metivier, 1980).
При изучении влияния стевиозида и стевиола на выделение инсулина изолированными клетками островков поджелудочной железы мышей установлено, что оба соединения стимулируют секрецию гормона (P. Jeppsen и соавт., 1996). Внутривенное введение стевиозида (2 г на 1 кг массы животного) крысам с инсулиннезависимым диабетом приводило к повышению секреции инсулина (но не глюкозы) в крови (P. Jeppsen и соавт., 1997).
Следует отметить, что гипогликемическое действие стевии наблюдается не всегда, часто носит кратковременный характер и требует дальнейшего изучения. Однако уже сейчас ясно, что продукт полезен для больных сахарным диабетом. Сохраняя \привычные вкусовые свойства пищевого рациона, стевия не приводит к повышению уровня сахара в крови даже в концентрации, в 10-15 раз превышающей ее среднесуточное потребление (С. Ovide и соавт., 1971; С. Maier и соавт., 1997; P. Jeppsen и соавт., 2000).
В некоторых странах мира употребление стевии стало привычным. Сладкую медовую траву можно употреблять без ограничений, ориентируясь только лишь на потребность организма в сладких продуктах; 1 кг сухого листа заменяет 30 кг сахара (при полном отсутствии калорий).
Гипотензивное действие. Способность стевиозидов понижать системное артериальное давление была обнаружена в ряде экспериментальных исследований (Е. Воеск, 1978,1986; G.Humbold и соавт. 1978; F. Machado и соавт., 1986). Доказан также диуретический эффект стевиозидов (М. Melis, 1996). Длительное использование стевиозидов вызывает кардиотонический эффект, оказывая положительное влияние на функцию сердечно-сосудистой системы.
Противомикробное действие. Результаты исследований подтверждают, что питательная среда с содержанием стевии замедляет рост Streptococcus mutans, Pseudomonas aeruginosa, Proteus vulgaris и др. (V. Yodyingyuand и соавт., 1977), а витамины и минералы, входящие в состав листьев стевии, необходимы для нормального функционирования иммунной системы. Для профилактики простудных заболеваний и гриппа рекомендуется употреблять чай со стевией. Установлена способность стевиозидов угнетать рост бактерий (Streptococcus sorbinus) в полости рта, благодаря чему стевиозиды можно использовать в качестве добавок к зубным пастам (Aguiar и соавт., 1987). Бактерицидные свойства стевии проявляются и при заживлении ран. Если неглубокую рану помазать концентратом стевии, она заживает без рубцов.
Применение стевии при ожирении. Являясь бескалорийной и обладая комплексом биологически активных веществ, нормализующих углеводный обмен в организме, стевия — незаменимый пищевой продукт для людей с избыточной массой тела. Некоторые пациенты отмечают снижение желания употреблять сладости и жирную пищу. Продукты со стевией входят в рацион многих диет для похудения. Не изменяя привычного образа жизни, получая наслаждение от приема пищи, содержащей стевию, люди с избыточной массой тела постепенно и безопасно худеют.
Влияние на органы пищеварения. Установлено положительное влияние стевии на органы пищеварительной системы. Стевия оказывает благотворный эффект на функциию поджелудочной железы и печени (A. Kinghom, D. Soejarto, 1991). В народной медицине Бразилии применяют чай со стевией при изжоге, усиленном газообразовании в кишечнике, снижении кислотности желудочного сока.
Влияние на кожу. Водный настой стевии является прекрасным косметическим средством для ухода за кожей, угнетает рост бактерий, вызывающих воспаление сальных желез и образование угрей. Маски из водного настоя стевии делают кожу мягкой, упругой, устраняют раздражение, препятствуют появлению морщин.
Дезинтоксикационное действие. Содержащиеся в стевии вещества обладают антиоксидантными свойствами (витамин С, р-каротин, минералы, Zn, Se). Мягкое диуретическое действие растения способствует выведению продуктов обмена, шлаков и солей тяжелых металлов из организма.
Общетонизирующее действие. Народный опыт применения стевии свидетельствует о ее способности восстанавливать силы человека после нервного и физического истощения. Благодаря синергизму и потенцированию компонентов, содержащихся в листьях стевии, ее применение устраняет усталость, повышает силовые и динамические характеристики мышц (D. Kinghorn, 1987). Все это делает стевию незаменимым продуктом для спортсменов и людей, занимающихся тяжелой физической или напряженной умственной работой. Стевия замедляет процессы старения.
18 сентября 1995 г. FDA дало заключение, что стевия может использоваться как "добавка к пище" в диетическом питании, но не как "пищевая добавка" в виде подсластителя для широкого применения в пищевых продуктах. Это значит, что стевия может продаваться как добавка к диете, способствующей улучшению здоровья. Данное решение противоположно принятому ранее, когда FDA определило, что стевия может быть использована только как продукт для наружного применения. Для более широкого применения в США было рекомендовано провести долгосрочные исследования для подтверждения безопасности препаратов стевии. Обоснованием такого решения были результаты хронических токсикологических исследований.
1. Через 6 мес введения экстракта стевии у самок наблюдалась протеинурия, а у самцов изменение количества эритроцитов. Через 12 мес такие изменения уже не наблюдались.
2. Через 6 мес введения экстракта концентрация глюкозы крови у самцов и самок повышалась. Этот вопрос требовал тщательной проверки.
3. Через 6 мес применения больших доз наблюдалось увеличение массы печени, почек, сердца, простаты и семенников у самцов и снижение массы яичников у самок. Через 12 мес значительной разницы между экспериментальными и контрольными группами не наблюдалось.
4. Морфологические изменения по отношению к контрольной группе животных проявлялись в снижении сперматогенеза, пролиферации интестинальных клеток семенников, пролиферации медуллярных клеток надпочечников, атрофии тимуса, изменениями в почках и прочее.
Необходимо отметить, что в перечисленных исследованиях экстракт стевии применялся в больших дозах. Одновременно был сделан вывод, что введение экстракта стевии самкам и самцам крыс F 344 на уровне 1 % с пищей на протяжении 2 лет (средний период жизни животных) не вызывает существенных нарушений. Поэтому в настоящее время сложно отрицать безвредность и полезные для здоровья свойства этого растения как пищевой добавки, которая, вероятно, будет зарегистрирована в США после завершения длительных исследований.
В настоящее время продукты стевии зарегистрированы во многих странах мира, включая Японию, Парагвай и Бразилию, а также в качестве диетической добавки к пище в США. В 1999 г.
Объединенный экспертный комитет по пищевым добавкам ВОЗ и Научный комитет по пищевым продуктам ЕС проанализировал имеющиеся данные по стевиозиду и определил, что он не может быть принят как сахарозаменитель до получения дополнительной информации, которая позволит определить суточную дозу потребления (Acceptable Daily Intake (ADI).
Перспективность применения сладких веществ стевии в пищевой и фармацевтической промышленности обусловлена тем, что среди других растительных подсластителей вкус стевии считается наиболее приятным и более близким ко вкусу к сахарозе, являясь при этом низкокалорийным продуктом. В 1991 г. Д.Г. Уванна писал, что "хотя вкус стевии приятен, он несколько отличается от вкуса сахара. Он больше напоминает вкус нектара дикой жимолости, слаще и несколько сильнее". При употреблении продуктов, в которых сахароза заменена стевиозидом, уменьшается поражаемость зубов кариесом, снижается масса тела у тучных людей, эти продукты можно употреблять людям, страдающим диабетом.
В Украине стевия зарегистрирована и применяется как сахарозаменитель в виде различных форм.
1. Как порошок из листьев для подслащивания чая, кофе или компотов.
2. Как пищевая добавка при изготовлении фруктовых компотов и джемов в пищевой промышленности.
3. Как пищевой подсластитель "сахарол", который был разработан ГНЦЛС (г. Харьков). Он представляет собой продукт с содержанием суммы дитерпеновых гликозидов не менее 70 %. Выдано разрешение для применения его в пищевой промышленности в качестве интенсивного подсластителя в виде столовых препаратов для больных сахарным диабетом или алиментарным
ожирением, а также при изготовлении диетических продуктов.
4. Путем очистки сахарола для пищевых целей в ГНЦЛС разработана также технология получения сахарола для медицинских целей, представляющего собой продукт с содержанием дитерпеновых гликозидов не менее 90 %. Показатели качества этого продукта находятся на уровне лучших зарубежных образцов.При изучении мутагенной активности сахарола в 4 тест-системах (на клетках костного мозга крыс, на плодовой мушке дрозофиле, в тесте Эймса и с помощью метода доминантной летальности в зародышевых клетках крыс) не было обнаружено отрицательных эффектов. Препарат не оказывал отрицательного влияния на репродуктивную функцию животных, не проявил эмбриотоксического действия. Введение крысам сахарола с пищей в течение 2,5 года не вызывало бластомогенного действия. Коммерческие препараты из стевии удобны для применения в пищевой промышленности; они достаточно термоустойчивы, не темнеют под воздействием высокой температуры, растворы препаратов не подвержены брожению, хорошо сочетаются с другими сахарами и органическими кислотами: лимонной, уксусной, молочной, яблочной, винной. Химические и микробиологические исследования показали исключительную стабильность стевиозида и ребаудиозида А в шипучих напитках.
Некоторые препараты из листьев стевии широко применяют для приготовления самых разнообразных продуктов питания: различных десертов, мороженого, вафель, жевательных резинок, газированных напитков, соусов, рыбных паст, диетических продуктов. Японские и бразильские потребители используют экстракт стевии как безопасный и бескалорийный естественный подсластитель в качестве пищевых добавок ко всем соусам сои, рассолам, кондитерским изделиям, спиртным напиткам. Традиционно стевия используется в виде измельченного травяного порошка, настойки, настоя, чая из самого растения или добавки к другим травяным чаям. Порошок листа стевии можно добавлять во все блюда, где обычно применяется сахар — каши, супы, напитки, чай, молоко, кефир, йогурты, кондитерские изделия и др. Для приготовления настоя берут 1 чайную ложку травяного порошка, заливают 250 мл кипятка и нагревают на водяной бане 15 мин, охлаждают при комнатной температуре, процеживают. Для приготовления чая берут 1/3 ложки травяного порошка, заливают 200 мл кипящей воды и настаивают 5-10 мин. Его используют как напиток на протяжении суток для утоления жажды.
Несмотря на детальную разработку получения сладких веществ из стевии и их промышленный выпуск, оснований для их медицинского применения как лекарственных средств, в частности для лечения диабета, недостаточно. Первые исследования, которые были проведены в 1993 г. в отделении лечебного и профилактического питания Украинского института гигиены питания (15 больных сахарным диабетом, 21 день), показали, что включение сахарола в диетическое питание положительно влияет на состояние больного. Но непосредственно сахароснижающий эффект не был зафиксирован. Аналогичные результаты были получены и в Институте эндокринологии и обмена веществ АМН Украины в отделении клинической фармакологии (30 больных, 30 дней). Стевия не проявляла лечебных свойств при сахарном диабете, но положительно влияла при включении в рацион диетического питания.
Таким образом, вышеизложенное свидетельствует о том, что дитерпеновые гликозиды стевии удовлетворяют требованиям, предъявляемым к заменителям сахара: имеют высокий коэффициент сладости, низкую энергетическую ценность, устойчивы при нагревании, легко растворяются и дозируются, утилизируются без включения инсулина, не оказывают вредного воздействия на организм. Однако говорить о применении гликозидов стевии как лекарственных средств еще преждевременно, так как для этого нет достаточно аргументированных оснований. Решение вопроса требует проведения дополнительных исследований.
Монеляин
Самые сладкие из всех известных плодов — это ягоды растения Dioscoreophyllum cumminsii Diets, которое растет в Западной Африке и имеет длинные волосяные вьющиеся стебли, как у виноградной лозы. Впервые оно было описано в 1895 г. Иглоподобная косточка плодов этого растения заключена в слизистую мякоть, обладающую сверхсладким вкусом. Поэтому эти плоды еще называют "ягоды радостной неожиданности". Установлено, что сладкий вкус обусловлен белковым веществом, которое авторы, открывшие его, назвали Монеллин в честь своего института (Monell Senses Center). Это был первый случай открытия в природе сладких белков. Для изучения свойств нового вещества из 1 кг фруктовой массы удалось выделить 3-5 г чистого мо-неллина. Его сладость в 2500 раз превосходила вкус сахарозы.
Молекула монеллина состоит из двух белковых субъединиц, каждая из которых в отдельности сладким вкусом не обладает. В дальнейшем при изучении последовательности аминокислот обнаружено, что на N-конце цепи А находится фенила-ланин. Особенностью молекулы является полное отсутствие гистидина. Также установлено, что человек и млекопитающие по-разному воспринимают сладкий вкус монеллина. Это вещество не токсично и не устойчиво к термической обработке. Сложность выделения монеллина ограничивает возможности его промышленного производства.
Тауматин
В 1839^. Даниэль обнаружил белок со сладким вкусом в "чудодейственных фруктах" растения Thaumatococus daniellii (Benth), растущего в Западной и Центральной Африке. Установлено, что ярко-красные плоды треугольной формы содержат сладкие белки в мембранной части семян. Они получили название тауматины (I и II). Отличие между ними заключается в разном строении амидного заместителя. Выход таумати-нов из 1 кг фруктов составляет 6 г. Сладость тауматинов в 1600 раз превышает сладкий, вкус сахарозы (J.D. Higginbotham, Hough, 1977, 1979). Обнаружено, что интенсивность сладкого вкуса значительно возрастает, когда молекулы тауматинов взаимодействуют с катионами алюминия. Компания Gale and Lyle Ltd разработала технологию получения такого соединения, которое назвали "талин", и начала его выпуск под торговым названием "тауматин-А1". В настоящее время талин, вероятно, является самым сладким веществом. Сладкий вкус вещества в 35 000 раз превышает вкус сахарозы, что делает его конкурентоспособным при промышленном производстве. Отрицательным свойством тауматинов и талина является их термолабильность. Они нашли применение при производстве соевых соусов, рыбных консервов, пикантных острых закусок, а также йогуртов, жевательных резинок, зубных паст и других продуктов.
Сладкие вещества из цитрусовых
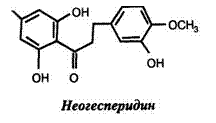 Было установлено, что флавоноиды цитрусовых после каталитического гидрирования приобретают сладкий вкус, а горечь исчезает. Оказалось, что в разных цитрусовых обнаруживаются различные флавоноиды: гесперидин — в апельсинах и лимонах, наригин — в грейпфрутах, а неогесперидин — в севильских апельсинах (табл. 21).
Было установлено, что флавоноиды цитрусовых после каталитического гидрирования приобретают сладкий вкус, а горечь исчезает. Оказалось, что в разных цитрусовых обнаруживаются различные флавоноиды: гесперидин — в апельсинах и лимонах, наригин — в грейпфрутах, а неогесперидин — в севильских апельсинах (табл. 21).
Модифицированные флавоноиды цитрусовых получили название дигидрохалконов. Они обладают сладким вкусом с ментоловым "холодком". Сладость гесперидина в 100 раз выше, чем у сахарозы, а у наригина — в 1000 раз. Неогесперидин слаще сахара в 1500-1800 раз. Установлено, что эти соединения менее токсичны, чем сахарин и цикламаты — дозы 0,2-1 г/кг не оказывали токсического эффекта.
Высокая сладость дигидрохалконов, их безвредность и низкая калорийность послужили основанием для широкого при менения в пищевой промышленности ряда стран. Так, в США неогесперидин использовали при изготовлении зубных паст, жевательных резинок, пищевых продуктов и безалкогольных напитков (Н. Beerens, Ann Fals. — Exp. Chem., 1968, 16, 108; R. T. Settzer - J. Chem. Eng News, 1975, 34, 27). В Венгрии их применяют при изготовлении фруктовых консервов, варенья и джемов для больных сахарным диабетом.
Таблица 21. Источники гидрохалконовых гликозидов (R.M. Horowitz, В. Gentili, 1978)
| Исходное вещество |
Растительный источник |
Конечный продукт |
| Неогесперидин (горький) Наригин(горький) Гесперидин(безвкусный) |
Севильский апельсин (Citrus aurantum) Грейпфрут (Citrus paradisi) Сладкий апельсин (Citrus sinensis), лимон (Citrus Limon) |
Неогесперидин дигидрохалкон (сладкий) Наригин дигидрохалкон (сладкий) Гесперидин дигидрохалкон (сладкий) |
Осладин
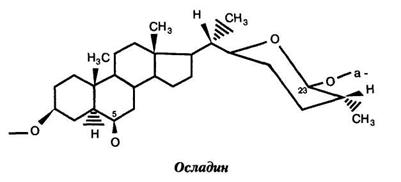
Жители Европы, Азии и Америки более тысячи лет знают о сладком вкусе корней папоротника Polypodium vulgare L, который широко распространен в лесах. Исследователям удалось выделить из этого растения вещество, обладающее сладким вкусом и имеющее строение стероидного сапонина. Его содержание в корнях очень незначительно (0,03%), однако по сладости оно превосходит сахарозу в 3000 раз. По строению осладин относится к двойным гликозидам, в молекуле которых стероидная структура соединена с одного конца с моносахаридом, а с другого — с дисахаридом. Такое строение напоминает структуру стевиозида (Gizbaj и соавт. — Chem. Ber, 1971, 104:837-846). При гидролизе осладина в кислой среде образуется a-L-рамнопираноза, p-D-глюкопираноза и агликон.
В настоящее время свойства осладина изучены мало, а его низкая концентрация в корнях является препятствием для широкого использования.
Малоизученные сладкие вещества
Целый ряд соединений неизвестной ранее структуры (ди-терпины), обладающие сладким вкусом, выделены японскими исследователями из канифоли сосны (Pinus). Некоторые из них в 1500-2000 раз слаще сахара. Безвредность этих веществ еще не изучена (Tahara A. et al. — Nature, 1971, 233, 619).
Из листьев чая (Hydrangea macrophylla) японскими исследователями Асахиро и Асано выделено сладкое вещество филодульцин, которое в 200-300 раз слаще сахарозы (Asahiro Y., Asano J., Chem.Ber., 1929, 62, 171). В 1978 г. описано получение аналога этого соединения. В дальнейшем эти исследования не получили развития.
В масле растения Perilla nanmnensis обнаружено вещество перилальдегид, обладающее в 12 раз более сладким вкусом, чем сахароза. Производное этого соединения, перилартин, по сладости превосходит сахар в 2000 раз. Однако оно обладает высокой токсичностью и не нашло применения в пищевой промышленности.
Плоды фруктов "Ло Хан" имеют дыневидную форму и распространены в Южном Китае. Их еще называют "трепало" (Swingle). Они имеют темно-коричневый цвет, тонкую кожуру и коричневато-серую волокнистую мякоть. В сушеном виде эти фрукты используются на протяжении многих лет в китайской народной медицине для лечения гриппа, воспаления горла, болезней желудка и кишечника, при отравлениях. Зеленые фрукты заготавливались в Китае в количестве более 1 тыс. т ежегодно. Вещество, обладающее сладким вкусом, удалось выделить из этих фруктов путем экстракции водой и 50 % этиловым спиртом. Его вкус напоминает сладость стевиозида, гли-цирризина или дигидрохалконов и сохраняется долго после 5-часового нагревания в воде. По интенсивности сладкого вкуса оно в 400 раз превосходит сахарозу. При изучении структуры этого вещества было установлено, что оно относится к тритерпеновым гликозидам с 5 или 6 глюкозными единицами (Lee С. Н., - Experientia, 1975,31, 533).
Известны также и другие сладкие продукты, свойства которых изучены еще недостаточно. Среди них можно назвать эрнандульцин — вещество не идентифицированной пока структуры, которое выделено из "сахарной травы", растущей в Мексике. Оно в 1000 раз слаще сахарозы. Потребление эрнандульцина в качестве сладости не приводит к тучности и является безвредным при сахарном диабете. Механизм его действия не изучен.
Представляет интерес также "морской" сахар, получаемый из морских растений. Он выпускается за рубежом в виде прутиков желто-зеленого цвета величиной со спичку. Считается превентивным средством развития атеросклероза.
Растительные модификаторы вкуса
К модификаторам вкуса относятся вещества, которые изменяют вкусовые ощущения. Наиболее известным из таких веществ является миракулин, выделенный более 100 лет назад из овальных фруктов красного цвета, растущих в Западной Африке на кустарнике Synsepalum duldficum Danielli. Он способен изменять вкусовые ощущения кислого. При этом лимон приобретает сладкий вкус, а уксус — вкус вина. Такой эффект сохраняется довольно долго. Поэтому плоды данного растения полумили название "чудодейственные" (англ. Miraculous — сверхъестественный, чудотворный, удивительный). Это растение было известно давно местным жителям Африки, которые жевали ягоды перед употреблением кислых фруктов.
Выделить миракулин в чистом виде было трудно, так как его содержание в плодах очень низкое и он чрезвычайно чувствителен к изменению рН среды. В настоящее время миракулин является наиболее изученным веществом белковой природы, способным вызывать изменение вкусового восприятия. Установлено, что это вещество относится к гликопротеидам и белковая часть молекулы играет существенную роль в восприятии сладкого вкуса. Изменение в белковой части молекулы ведет к потере специфических свойств. Сладкий вкус кислых продуктов наблюдался при концентрации миракулина 5-10~8 М и достигал максимума при 4-10~7 М, медленно убывая в течение 2 ч.
Высказано несколько предположений относительно механизма действия миракулина. Одни авторы считают, что он способен одной частью молекулы блокировать рецепторы, воспринимающие кислый вкус, а другой — вызывать восприятие сладкого вкуса (Dzendocet E., — Percept Psychophys, 1969, 6, 187). Другие — что в кислой среде белковая молекула этого вещества изменяется таким образом, что участки, содержащие ксилозу и арабинозу, получают возможность взаимодействовать с рецепторами сладкого вкуса (Kurihara К., Beidler L. М„ — Nature, 1969, 222, 1176). Высказано также предположение, что миракулин обладает свойством усиливать сладкий вкус (А. Крутошикова, М. Угер, 1988).
В 70-х годах американская фирма Miralin Corporation освоила промышленное выращивание растения, содержащего миракулин, и начала производить концентрат из его фруктов. Применяли его перед приемом продуктов или включая в продукты питания. Однако в 1977 г. регламентирующие органы США запретили выпуск любых продуктов, содержащих миракулин.
Артишок (Cynara scolymus) — многолетнее растение из семейства сложноцветных. По внешнему виду он напоминает чертополох, но имеет более крупные соцветия синего цвета. В пищу употребляют мясистое цветоложе и нижние части чешуи молодых, еще не раскрытых соцветий с удаленными цветками. По вкусу сырой артишок напоминает недозрелые грецкие орехи и считается деликатесом. В диком виде артишок встречается в Африке, на юге Европы и в Южной Америке. Как питательное и целебное растение он был известен еще 5 тысячелетий тому назад в Древнем Египте и очень ценился в Древнем Риме.
Впервые культивировать этот овощ начали в Италии, оттуда в XV в. он распространился по всей Западной Европе. Особенно понравился артишок населению Франции. В питании артишок используют в сыром, вареном и консервированном виде. В народной медицине его применяют для лечения атеросклероза, нарушений желчеотделения и работы почек, сахарного диабета. Артишок стимулирует аппетит, по-видимому, за счет сахароснижающего эффекта, применяется при снижении аппетита у стариков и детей. В научной медицине артишок рекомендуют как диетическое средство при сахарном диабете, атеросклерозе, заболеваниях печени и почек, при истощении.
Давно было отмечено, что артишок обладает способностью модифицировать вкусовые ощущения, подобно миракулину. Если предварительно прополоскать рот экстрактом из артишока, то растворы поваренной соли, сахара, лимонной кислоты и хинина вызывают одинаковые ощущения сладкого, которое сохраняется в течение 4-5 мин (Bartoshuk L.M., Lee C.H., Scarpellino R., —Science, 1972, 178, 988). При изучении химического состава растения было установлено, что он содержит 2 % белка, инулин, витамины С и В, а также хлорогеновую кислоту и синарин, которые обусловливают эффект модификации вкуса.
Благодаря описанным свойствам при добавлении к пищевым продуктам артишок улучшает их вкусовые качества. Однако эти свойства не нашли пока широкого применения и он не используется в пищевой промышленности.
К модификаторам вкуса также относится растение Gymnema sylvestris R Br., которое распространено в южных странах и издавна используется в народной медицине для лечения сахарного диабета как сахароснижающее средство. Эти эффекты подтверждены в настоящее время экспериментально. Местные жители давно заметили, что если пожевать листья этого растения, то пропадает восприятие вкусовых ощущений. Любая пища (горькая, соленая, сладкая или кислая) становится безвкусной, напоминая вкус мела. Однако терпкий и острый вкус не изменялись.
/Веществом, ответственным за этот эффект, оказалась гимнемовая кислота, которую удалось выделить из листьев растения. Свойства растения и гимнемовой кислоты не нашли практического применения. У нас возникала идея использовать вещество, после предварительного изучения, при проведении глюкозотолерантного теста, когда исследуемому приходится выпивать относительно большой объем жидкости приторно-сладкого вкуса. Однако эта идея из-за отсутствия сырьевой базы не была реализована.
Имеются сведения и о других малоизвестных растениях — модификаторах вкуса. Так, в Средней Азии, Закавказье, Индокитае, Индостане, Иране и Северной Африке встречается растение Zyzyphus jujuba Mill, унаби, семейства крушиновых. Это кустарник с красно-коричневыми ветвями в узлах и острыми шипами длиной около 3 см. Он обладает съедобными красно-коричневыми плодами с косточкой, которые в виде отвара применяются в народной медицине как слизистое и обволакивающее средство при кашле, бронхите и коклюше. Если пожевать лист этого растения, а потом положить на язык сахар, то последний станет безвкусным. Даже если попробовать сахарин, который в 500 раз слаще сахара, ощущение сладкого не возникнет. Было установлено, что кроме сладкого пропадает восприятие горького, кислого, соленого и острого, а чувствительность к болевым воздействиям сохраняется. Модификатором вкуса является гликозид, присутствующий в листьях зизифуса и нейтрализующий вкусовые ощущения.
Известно также африканское растение дика, или ассаа, которое не только притупляет вкус кислого, но способно усиливать аппетит, делая пищу вкусной. Такое действие сохраняется в течение часа.
Необходимо отметить, что все описанные модификаторы вкуса еще не нашли широкого практического применения и редко используются в пищевой промышленности.
Сладкие спирты
Сахаридные спирты (полиолы) содержатся в некоторых растениях, а для промышленных целей их получают искусственно из восстанавливающих моносахаридов. При восстановлении как альдоз, так и кетоз образуются одинаковые полиолы, однако из кетоз дополнительно получается стереоизомерный спирт. В частности, восстановление D-глюкозы приводит к образованию D-сорбита, а восстановление D-фруктозы — к одновременному образованию D-сорбита и D-маннита. Описаны различные методы восстановления моносахаридов в полиолы. Согласно женевской номенклатуре, названия спиртов производятся от названий углеводородов с присоединением окончания "ол". Кроме того, спирты имеют также эмпирические названия.
Важной особенностью действия многоатомных спиртов (по-лиолов) является их медленное всасывание в кишечнике (в 5-6 раз медленнее, чем глюкозы). Это связано с тем, что они адсорбируются путем простой диффузии за счет разницы градиента концентрации в кишечнике и крови, а не с помощью переносчиков и активаторов. Медленно всасываясь, многоатомные спирты создают высокое осмотическое давление в кишечнике, обусловливая прилив и задержку жидкости, что, в свою очередь, вызывает разжижение кишечного содержимого и усиление перистальтики ("осмотический понос"). Поэтому их суточная доза не должна превышать 30 г (для лиц пожилого возраста — 15-20 г), более высокие дозы оказывают послабляющий эффект, вызывают тошноту и даже рвоту (P. Peters, R. Look, 1958).
В 2002 г. Американская диабетическая ассоциация в опубликованных рекомендациях по диетическому питанию констатировала, что сахарные спирты вызывают менее выраженный постпрандиальный подъем глюкозы, чем фруктоза, сахароза и глюкоза, а также имеют более низкую энергетическую ценность (Diabetes Care, 2002, 25 (suppl.l): S. 50-60).
Употребляя эти вещества, необходимо выполнять следующие правила:
1) при использовании ксилита и сорбита следует начинать с небольших доз (10-15 г в сутки) для определения индивидуальной переносимости, в том числе и послабляющего эффекта;
2) применение полиолов рекомендуется на фоне компенсации или субкомпенсации сахарного диабета;
3) нужно учитывать калорийность сахарозаменителей;
4) при появлении тошноты, вздутия живота, изжоги доза сахарозаменителя должна быть уменьшена до 10-15 г или его нужно отменить.
Сорбит
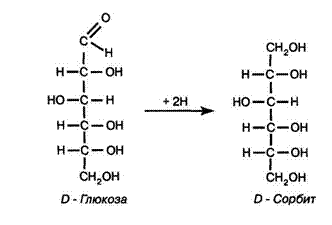 Среди шестиатомных спиртов, имеющих сладкий вкус, наиболее широкое применение получил сорбит. Он был открыт французским химиком Boussingault в 1868 г. при исследовании ягод рябины. Ему удалось выделить вещество, сходное с маннитом и дульцитом, которое автор подробно описал и присвоил ему название сорбит (по-французски le sorb — рябина, а по-латыни — Sorbus aucuparia L). В последующем сорбит был обнаружен в небольших количествах и в других ягодах и фруктах. Наибольшее его количество обнаружено в ягодах рябины и терна (от 0,5 до 10 %), а также боярышника (4,7-7,6 %) и кизильника (3,6-5,1 %). При созревании плодов содержание сорбита увеличивается, а при хранении он превращается во фруктозу. Кроме того, сорбит обнаружен в листьях как низших, так и высших растений. Он является промежуточным продуктом при синтезе крахмала, целлюлозы, фруктозы, сорбозы и аскорбиновой кислоты. Его выявили в отходах сахарного производства (Т. Dalkowski и соавт., 1966).
Среди шестиатомных спиртов, имеющих сладкий вкус, наиболее широкое применение получил сорбит. Он был открыт французским химиком Boussingault в 1868 г. при исследовании ягод рябины. Ему удалось выделить вещество, сходное с маннитом и дульцитом, которое автор подробно описал и присвоил ему название сорбит (по-французски le sorb — рябина, а по-латыни — Sorbus aucuparia L). В последующем сорбит был обнаружен в небольших количествах и в других ягодах и фруктах. Наибольшее его количество обнаружено в ягодах рябины и терна (от 0,5 до 10 %), а также боярышника (4,7-7,6 %) и кизильника (3,6-5,1 %). При созревании плодов содержание сорбита увеличивается, а при хранении он превращается во фруктозу. Кроме того, сорбит обнаружен в листьях как низших, так и высших растений. Он является промежуточным продуктом при синтезе крахмала, целлюлозы, фруктозы, сорбозы и аскорбиновой кислоты. Его выявили в отходах сахарного производства (Т. Dalkowski и соавт., 1966).
В 1929 г. Thannhauser и Meyer показали, что при введении сорбита экспериментальным животным не наблюдается повышения концентрации глюкозы в крови, и предложили использовать его как заменитель сахара. По сравнению с сахарозой, интенсивность сладкого вкуса сорбита составляет 0,6, калорийность близка к сахарозе — 3,54 ккал/г, а энергетическая ценность 16,3 кДж/г. Поэтому его следует ограниченно рекомендовать больным с избыточным весом.
Сорбит представляет собой бесцветные кристаллы сладкого вкуса, хорошо растворимые в воде, горячем и холодном спирте. Получают сорбит путем каталитического восстановления D-глюкозы. Он является промежуточным продуктом при синтезе аскорбиновой кислоты.
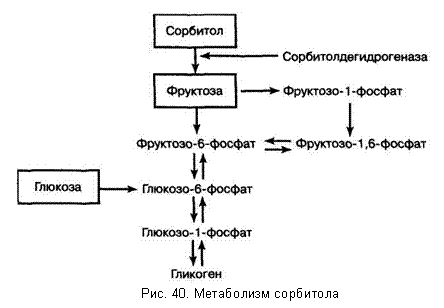
При пероральном применении до 3 % сорбита выводится с мочой в неизмененном виде. С калом сорбит не выделяется или выделяется в незначительном количестве (L.H. Adcock, С.Н. Gray, 1956; N. Ertel и соавт., 1983). Метаболизируется сорбит в печени под действием фермента сорбитолдегидрогеназы, превращаясь во фруктозу, которая затем включается в общий цикл обмена углеводов (рис. 40). Как указывалось выше, при сахарном диабете наблюдается эндогенное образование сорбита из глюкозы при помощи фермента альдозоредуктазы, что связывают с развитием ангио- и нейропатий, ретинопатии и катаракты (А.С. Ефимов и соавт., 1984).
 Показано, что содержание сорбита, глюкозы и фруктозы в тканях периферической нервной системы повышается при гипергликемии. Другие авторы установили, что у больных диабетом с почечной недостаточностью уровень сорбита и маннита в сыворотке крови повышен. Кроме того, ряд авторов обнаружили у больных диабетом повышение экскреции с мочой сорбита, га-лактита и маннита, что коррелировало со степенью глюкозурии.
Показано, что содержание сорбита, глюкозы и фруктозы в тканях периферической нервной системы повышается при гипергликемии. Другие авторы установили, что у больных диабетом с почечной недостаточностью уровень сорбита и маннита в сыворотке крови повышен. Кроме того, ряд авторов обнаружили у больных диабетом повышение экскреции с мочой сорбита, га-лактита и маннита, что коррелировало со степенью глюкозурии.
В связи со сложившимися представлениями о роли сорбитолового шунта в развитии осложнений диабета, возникли опасения применения субстратов полиолового пути обмена Сахаров, в особенности сорбита и фруктозы. При этом высказывалось мнение, что опасен сорбит, образующийся эндогенно, а введенный продукт хорошо усваивается организмом и не опасен. В то же время имеются сообщения, заставляющие отнестись с осторожностью к этому утверждению. Так, при скармливании крысам пищи, содержащей 30 % сорбита, через 40 дней в их печени наблюдалось снижение активности сорбитолдегидрогеназы на 50 %. При этом отмечалось усиление синтеза гликогена на фоне угнетения гликолиза и активности полиолового пути.
В других исследованиях при введении крысам сорбита, меченного радиоактивным изотопом, в ежедневной дозе 100 мг наблюдалось значительное повышение его концентрации в хрусталиках глаза. Одновременно обнаруживалось также повышение содержания глюкозы и фруктозы, что свидетельствует о возможности их образования из сорбитола (E. Loten и соавт., 1966). Однако на основании этих данных окончательные выводы делать преждевременно, так как в описанных случаях применялись высокие дозы сорбита. Необходимо учитывать их при составлении диеты и не рекомендовать больным прием этого заменителя длительное время. Показано, что прием сорбита в дозе 100 г вызывает у здоровых людей незначительное повышение гликемии, а прием 25 г 3 раза в день не приводил к существенным изменениям этого показателя (Л.Г. Шерман, 1967; А.Н. Карамышев, 1972).
Было установлено, что сорбит обладает целым рядом положительных свойств. Доказано, что у больных диабетом он усваивается лучше, чем глюкоза, так как, превращаясь во фруктозу, не требует для этого инсулина и способствует накоплению гликогена в печени (но не мышечной ткани). Кроме того, он обладает антикетогенным действием, что представляет практический интерес в связи со склонностью больных сахарным диабетом к кетоацидозу. По данным некоторых авторов, внутривенное введение ксилита и сорбита детям при лечении кетонемии не требовало увеличения дозы инсулина, в то время как применение обычных углеводов сопровождалось ее повышением.
Сорбит благоприятно влияет на деятельность желудочно-кишечного тракта, стимулирует выделение желудочного сока и обладает желчегонной активностью. Последнее свойство также имеет определенное значение при назначении сорбита больным сахарным диабетом, так как при этом заболевании в некоторых случаях наблюдается тенденция к атонии желчных путей (П.Н. Майструк, Я.Л. Германюк, 1983). Улучшение оттока желчи, устранение ее застоя значительно облегчает состояние больного. Сорбит с успехом применяли при острых и хронических заболеваниях печени. При его употреблении отмечается значительное улучшение уже на 2-3-й день. Исчезают или уменьшаются боли, чувство давления в правом подреберье, горечь во рту, тошнота, нормализуется стул, улучшаются аппетит, сон. Разработаны рекомендации приема сорбита при хроническом запоре. Как желчегонное и послабляющее средство его следует принимать до еды или через 1-2 ч после нее по 5-10 г 2-3 раза в день. Обычно максимальная доза в сутки составляет 20-30 г. Если начинается понос, нужно уменьшить либо дозу сорбита, принимаемую в один раз, либо число приемов. Иногда предпочитают принимать сорбит в растворенном виде (50 г пищевого сорбита растворяют в 0,5 л воды). В стакане такого раствора будет находиться 20 г пищевого сорбита. Принимать его можно по 1/4-1/2 стакана 2-3 раза в день. Готовить его лучше не больше чем на 2 дня. В результате многократного применения сорбита установлено, что у больного человека имеется слабительный порог, который индивидуален у каждого. Так, у многих лиц доза 7-10 г вызывала послабляющий эффект, в то время как другие не реагировали на дозу в 50 г (П.Ф. Крышень, Ю.И. Рафес, 1979). Необходимо отметить, что желчегонные и послабляющие свойства у сорбита выражены в меньшей степени, чем у ксилита.
Сорбит нашел применение при диагностических исследованиях, в частности для определения функции опорожнения желчного пузыря (Т.А. Куклина, 1967; В.В. Китаев, 1968). Обычно с этой целью используют в качестве раздражителей различные вещества: яичный желток, оливковое масло, сернокислую магнезию и др. Они раздражают слизистую оболочку двенадцатиперстной кишки, вызывают повышение секреции гормона холецистокинина, который расслабляет сфинктер Од-ди и сокращает желчный пузырь. Сорбит использовали в бариево-сорбитной смеси при рентгенологическом исследовании желудочно-кишечного тракта для ускорения перистальтики и прохождения рентгеноконтрастного вещества, что значительно сокращало время процедуры. Сорбит также применяли с целью проведения слепого зондирования. При этом продемонстрированы его преимущества перед сернокислой магнезией (Ю.И. Рафес, 1968).
Интересно свойство сорбита уменьшать потребность организма в витаминах группы В, что, вероятно, связано с повышением их синтеза в кишечнике вследствие изменения бактериальной флоры (К. Okuda, 1961).
Так как сорбит не всасывается почечными канальцами и во время кругооборота в организме "забирает" воду из межклеточных пространств, то благодаря осмотическому действию проявляет диуретический эффект (A. Leimdorter, 1954), который может быть использован для обезвоживания и дезинтоксикации при отеке легких, остром серозном плеврите, уремии. Противоотечное действие сорбита было использовано и в глазной практике у больных глаукомой, так как отмечено, что при внутривенном введении препарата наблюдается снижение внутриглазного давления.
Многократное клиническое применение сорбита выявило также целый ряд его недостатков. Так, длительное употребление в больших количествах может в редких случаях вызвать тошноту, вздутие живота, изжогу, легкое головокружение и даже появление сыпи. В таких случаях следует отказаться от его использования.
К недостаткам сорбита как сахарозаменителя относятся его более низкая сладость по сравнению с сахарозой и специфический "металлический" привкус. При замене сахара, чтобы сохранить сладость, сорбит необходимо добавлять в двойном количестве, что приводит к увеличению калорийности. У больных сахарным диабетом после применения сорбита иногда наблюдается повышение уровня молочной кислоты в крови, а при средней и тяжелой формах этого заболевания — значительное повышение глюкозы крови. При рекомендуемом добавлении сорбита в пищу в количестве 30 г его энергетическая ценность составляет 120 ккал, что необходимо учитывать при расчете суточной калорийности пищевого рациона.
Пищевой сорбит находит применение в кондитерской промышленности. Его используют вместо сахара в печенье, вафлях и других продуктах, предназначенных для больных сахарным диабетом. Высокая гигроскопичность сорбита, его способность удерживать воду очень ценна в кондитерском производстве для сохранения свежести изделий. Конфеты, помадки, мармелад, к которым добавлено 5-15 % сорбита, практически не высыхают. Благодаря свойству задерживать воду сорбит является прекрасным стабилизатором влажности в продуктах питания при разных климатических условиях в течение длительного времени. Особое значение в этом отношении приобрел жидкий сиропообразный раствор сорбита, который не теряет свойств при варке, улучшая качество и стабилизируя концентрацию фруктовых соков, конфет, варенья.
При употреблении сорбита и содержащих его кондитерских изделий следует учитывать содержание в них муки, жиров и других добавок, которые могут повлиять на гликемический профиль и калорийность диеты. Считается, что применение сорбита может быть длительным, однако целесообразно делать месячные перерывы через каждые 3-4 мес после его употребления. Желательно чередовать прием сорбита с другими некалорийными сахарозаменителями.
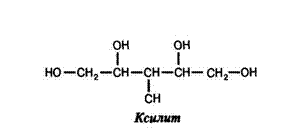
Ксилит
Ксилит относится к пятиатомным спиртам. Он представляет собой белые кристаллы без запаха, хорошо растворяется в воде и по сладости не отличается от сахара. По сравнению с сахарозой интенсивность его сладкого вкуса составляет 0,85-1,2. Ксилит обнаружили в березовом соке, малине, клубнике и других ягодах и фруктах. Калорийность ксилита равна около 4,0 ккал/г, а энергетическая ценность — 16,98 кДж/г. Кристаллический ксилит вызывает холодящее ощущение на языке, которое объясняется отрицательной теплотой его растворения. Впервые ксилит был получен в виде сиропа Бертраном и Фишером в 1891 г. путем восстановления ксилозы амальгамой натрия, поэтому он долгое время характеризовался в литературе как сироп, и только в 1960 г. одна из американских фирм начала выпуск кристаллического ксилита.
 В настоящее время ксилит получают путем гидролиза из хлопковой шелухи или кукурузных кочерыжек. В Финляндии ксилит получают из березовой коры. Процесс состоит из двух стадий —гидролиза полисахаридов сырья до образования ксилозы и восстановления последней до ксилита. Его производство возможно на действующих сахарных заводах без изменения технологического процесса.
В настоящее время ксилит получают путем гидролиза из хлопковой шелухи или кукурузных кочерыжек. В Финляндии ксилит получают из березовой коры. Процесс состоит из двух стадий —гидролиза полисахаридов сырья до образования ксилозы и восстановления последней до ксилита. Его производство возможно на действующих сахарных заводах без изменения технологического процесса.
Вкус ксилита ощущается большинством людей как приятный, не отличающийся от вкуса сахарозы. При введении в организм он всасывается более медленно, чем глюкоза, составляя 15-20 % скорости всасывания последней. Поэтому при употреблении больших доз ксилита он длительное время задерживается в кишечнике, в результате чего в нем накапливается большое количество жидкости, усиливается перистальтика и возникает понос.
Иногда в первые дни употребления ксилита отмечается незначительный метеоризм (вздутие живота), расстройство кишечника. Если это продолжается несколько дней, надо уменьшить дозу ксилита. Введенный ксилит почти полностью всасывается в кишечнике, выведение его с калом и мочой незначительно. У здоровых людей количество выделенного с мочой ксилита после приема внутрь 40 г составило 0,1-1,2 г, т.е. не более 3 % принятой дозы. Содержание ксилита в крови, как правило, очень невысоко и колеблется в пределах 0-16 мг%. Его концентрация в крови может повышаться после введения в организм некоторых веществ. Так, более резкое и длительное увеличение содержания ксилита в крови и выделения его с мочой наблюдалось после приема этанола. Уже через 3 ч после введения 60 г спирта уровень ксилита в крови достигал 0,15-0,38 мг%, а выделение с мочой — 18-63 мг. При внутривенном введении этанола эти показатели увеличивались в крови до 0,25-0,6 мг%, а в моче — до 17,5-83 мг. Механизм этого явления не изучен.
По мнению ряда авторов, быстрота и большее пространство распределения ксилита (примерно 40 % массы тела) по сравнению с глюкозой свидетельствуют о том, что его поступление в клетки не связано с транспортными механизмами, в частности, инсулин не оказывает влияния на его проникновение в клетку.
Большая часть введенного ксилита метаболизируется в печени (S. Segal, В. Foley, 1959; М. Spitzl и соавт., 1970). На втором месте стоят почки, затем сердце, р*-клетки поджелудочной железы, надпочечники и головной мозг. В жировой ткани ксилит может превращаться в липиды. В печени он окисляется в ксилозу. У людей пожилого возраста ксилит усваивается несколько хуже, чем у молодых.
Следует подчеркнуть, что ксилит является естественным промежуточным продуктом углеводного обмена у людей и животных. Эта пентоза после фосфорилирования включается в пентозофосфатный шунт, где в сочетании с рибулезо-5-фосфа-том образует седогептулезо-7-фосфат, затем фруктозо-6-фос-фат и фосфоглицеральдегид, которые вступают в гликолити-ческий путь. Было установлено, что в организме наряду с пентозофосфатным циклом, в котором окисляется ксилит, существует гексозофосфатный цикл, называемый еще циклом "глюкуроновая кислота — ксилулоза". В этом цикле ксилит занимает промежуточное положение, а конечным продуктом его окисления является углекислый газ. В процессе окисления ксилита образуется 35 эквивалентов АТФ, что на 10 % больше, чем при метаболизме глюкозы. Установлено, что при экспериментальном диабете скорость обмена ксилита возрастает пропорционально тяжести заболевания. При тяжелой форме она увеличивается в 4 раза, что свидетельствует о возможности использования ксилита в качестве источника энергии.
Несколько слов следует сказать о ксилозе, которая в организме может превращаться в ксилит, а последний может метаболи-зйроваться в ксилозу, которая обнаруживается в моче при пен-тозурии. При введении в организм большая часть ксилозы, в отличие от ксилита, выводится, с мочой. В природе ксилоза встречается преимущественно в виде D-изомера. Она обнаруживается в составе полисахаридов древесины (в частности, в ксилане древесины), в различных гликозидах и олигосахаридах. В организме человека и животных D-изомер ксилозы входит в состав гликозаминогликанов соединительной ткани. Поэтому, вероятно, избыточное поступление или накопление ксилозы в организме может приводить к нарушению ее функции. Установлено, что введение ксилозы в больших количествах молодым экспериментальным животным вызывало развитие катаракты. Интересно было бы изучить, не оказывает ли влияние этот моносахарид на возникновение катаракты при сахарном диабете.
Ксилит, не являясь чужеродным веществом для организма, обладает низкой токсичностью и хорошей переносимостью. По данным литературы, ксилит не оказывает заметного влияния на содержание сахара в крови у здоровых и больных сахарным диабетом. Наибольший подъем уровня глюкозы в крови у здоровых лиц после приема 40 г ксилита внутрь составлял 20 мг%. При пероральном введении ксилита (16-20 г в день) или после внутривенного введения не обнаружено значительного подъема уровня глюкозы в крови и отсутствия глюкозурии в моче. Кроме того, при глюкозурии 20-40 г в сутки введение ксилита приводило к снижению содержания сахара в моче. Нагрузка 30 г ксилита с последующим определением гликемии каждые 30 мин не вызывала у людей подъема уровня сахара в течение 3 ч (М.Н. Егоров, Н.М. Цирюльников).
В экспериментальных исследованиях было доказано, что сорбит и ксилит равноценны в качестве предшественников гликогена в печени здоровых крыс и животных с экспериментальным диабетом. Доказать синтез гликогена в мышцах из ксилита и сорбита не удалось.
По данным некоторых авторов, ксилит способствует выработке инсулина. Подобный эффект получен в опытах in vitro, однако он был выражен слабее, чем при действии глюкозы. Установлено, что при внутривенном введении животным ксилита (собаки, коровы, козы, крысы, кролики, лошади) наблюдается стимуляция выработки инсулина, выраженность которой зависит от вида животного и дозы препарата (Т. Kuzuya и соавт., 1969, 1971). Подобный эффект некоторые авторы наблюдали и у людей. При этом уровень сахара крови изменялся незначительно. Кроме того, удалось установить, что ксилит обладает способностью снижать уровень неэстерифицированных жирных кислот.
Отмечено выраженное антикетогенное действие ксилита. Ксилит усиливал поглощение кислорода и подавлял образование ацетоуксусной кислоты тканью печени (В.Р. Клячко и со-авт., 1968). Известно, что антикетогенное действие связано с уменьшением образования в печени ацетил-Ко А, являющегося источником образования кетоновых тел.
Высказано несколько предположений о возможном механизме этого эффекта.
1. Метаболизируясь по пентозофосфатному пути, ксилит способствует образованию глицерофосфата, принимающего участие в синтезе триглицеридов, и вовлекает в этот процесс свободные жирные кислоты. При этом их окисление в ацетил-КоА снижается.
2. При метаболизме ксилита по пентозофосфатному пути повышается образование НАДФН, который стимулирует синтез жирных кислот из ацетил-Ко А, снижая его содержание.
3. Повышая интенсивность гликолиза, ксилит способствует усилению образования пировиноградной кислоты, которая превращается в щавелевоуксусную, способствующую окислению ацетил-Ко А в цикле Кребса.
4. Ксилит (а также сорбит и глицерин), в отличие от глюкозы, уменьшает окисление свободных жирных кислот, которое повышено при сахарном диабете вследствие снижения интенсивности метаболизма углеводов.
5. Антикетогенный эффект ксилита и сорбита может быть обусловлен усилением гликогенообразования в печени, что снижает распад жиров и их поступление с периферии.
Изучение свойств ксилита показывает, что его применение не может быть ограничено только использованием в качестве заменителя сахара для больных диабетом. Имеется опыт его применения с диагностической и лечебной целью при заболеваниях желчевыводящих путей как средства, способствующего рефлекторному сокращению желчного пузыря при тюбаже и рентгенологическом исследовании желчного пузыря и желчных путей (холеграфия и холецистография). Анализ рентгенологических исследований свидетельствует о том, что ксилит может широко использоваться в клинике как холекинетическое средство, вызывающее интенсивное сокращение стенок желчного пузыря без побочных явлений. В этом его преимущество перед общепринятыми физиологическими раздражителями (яичные желтки, сметана и т.д.) (П.Ф. Крышень, Ю.И. Рафес, 1979).
Способность ксилита повышать образование гликогена в печени и желчегонные свойства послужили основанием для его применения при заболеваниях печени. При этом у больных холециститом исчезают или уменьшаются боли и чувство давления в правом подреберье, горечь во рту, тошнота, нормализуется стул, улучшаются аппетит, сон. Как желчегонное и послабляющее средство ксилит назначают по 10-20 г на прием. Лучше всего употреблять эту дозу натощак, тогда эффект более выражен. Доза не должна превышать 0,5 г на 1 кг массы тела, что примерно составляет 30-35 г (П.Ф. Крышень, Ю.И. Рафес, 1979). Можно применять ксилит для так называемого гуманного тюбажа, широко распространенного метода "промывания" желчных путей. В 1/2 стакана теплой воды растворяют 10-15 г ксилита, дают больному, после чего он лежит на правом боку с грелкой в течение 1-1,5 ч.
Являясь прекрасным источником энергии и обладая к тому же независимым от инсулина метаболизмом, антикетогенным и липотропным действием, ксилит получил широкое применение в качестве средства для парентерального питания у больных, особенно перенесших операции на желудочно-кишечном тракте.
Отмечено стимулирующее влияние ксилита на функцию коры надпочечников, когда содержание 11-оксикортикостеро-идов под влиянием преднизолонотерапии было значительно сниженным (М. Onuki, 1971). Положительные результаты были также получены при внутривенном введении 10 % раствора (30 г в сутки) больным нефрозом, гипертиреозом, ревматизмом, эритродермией (Н.В. Ким, 1971).
Э.М. Кречетникова (1970) на фоне атеросклеротической диеты назначала 40 г ксилита ежедневно 36 больным с выраженным атеросклерозом и коронарной недостаточностью. Автор отмечала исчезновение болевых симптомов, особенно у больных с частыми и упорными приступами стенокардии. Другие авторы, применяя 10 % раствор ксилита (50 мл внутрь 3 раза в день) для лечения 32 больных с коронарным атеросклерозом, обнаружили статистически достоверное снижение содержания холестерина и липопротеидов (А.Б. Шахназарова, Н.В. Лукаша, 1970, Л.И. Чунакова, 1971). В некоторых исследованиях у лиц с вегетативно-сосудистой дистонией и склонностью к гипертензии наступало ухудшение состояния, сопровождавшееся повышением артериального давления. Поэтому автор не рекомендует назначение ксилита лицам с сопутствующей гипертонической болезнью. Кроме того, пожилым людям не рекомендуют в течение длительного времени ежедневно употреблять ксилит. Он может усилить атеросклеротические изменения в кровеносных сосудах. Его следует применять в течение коротких промежутков времени и сочетать с другими сахаро-заменителями. Употреблять ксилит не рекомендуется при колитах со склонностью к поносам.
В исследованиях, проведенных на добровольцах, получавших на протяжении 2 лет диету с ксилитом, констатировано, что данный нутриент не вызывал в крови изменений концентрации глюкозы, инсулина, триацилглицерина, холестерина, липопротеидов, белков, урата, лактата, креатинина, активности аминотрансфераз и аминопептидаз. Кроме того, не обнаружено отклонений от нормы в содержании ряда ингредиентов в моче. При этом ксилит в 9 раз снижал заболевание кариесом.
С учетом того, что ксилит не оказывает выраженного гипергликемического эффекта, способствует накоплению гликогена в печени, метаболизируется независимо от инсулина, используется организмом в качестве источника энергии, обладает анти-кетогенным действием и относительно приятным вкусом, он имеет определенные преимущества перед другими калорийными заменителями сахарозы. Кроме того, послабляющее и желчегонное действие дополняют его положительные свойства (И.В. Домарева, 1967; М.И. Мартынов и соавт., 1971; М.В. Милишникова, 1969).
Наблюдения показали, что под влиянием курсового лечения ксилитом значительно улучшалось общее состояние больных диабетом. Большинство из них отмечали прилив сил, бодрость, уменьшение или полное исчезновение общей слабости, в том числе и мышечной скованности, головной боли, головокружения. Уменьшались или полностью исчезали диабетические жалобы: сухость во рту, жажда и в ряде случаев кожный зуд. Лечение ксилитом способствовало улучшению аппетита, уменьшению или полному исчезновению болей и тяжести в правом подреберье, а также ряда диспептических жалоб (горечи во рту, тошноты).
Ксилит применяется больными сахарным диабетом в чистом виде, а также в виде кондитерских изделий (конфет, шоколада, вафель и др.). Пищевые продукты, содержащие ксилит, не плесневеют. В то же время их применение должно учитываться у больных сахарным диабетом в соответствии с калорийностью диеты (Л.С. Маримьян, 1961). Многие больные сахарным диабетом готовят варенье и джемы на ксилите, которые сохраняют вкусовые качества ягод и фруктов. На ксилите приготавливаются фруктовые воды, мороженое и другие изделия. Но ксилит в 10 раз дороже обыкновенного сахара, у него нет столь обильных источников сырья, как сахарная свекла и сахарный тростник, что затрудняет его широкое распространение.
Комитет по продуктам питания ЕС рассмотрел результаты исследований по метаболизму, острой, субхронической и хронической токсичности ксилита на крысах и собаках, проанализировал возможные отклонения в развитии на трех поколениях крыс, а также данные тератогенности и мутагенности (in vitro и in vivo). Учтены также выводы проведенных широкомасштабных исследований по толерантности к ксилиту, принятому внутрь. При этом было констатировано, что ксилит не обладает генотоксичностью. Данные, полученные при применении его у людей, не дают оснований ожидать вредных последствий от выведения с мочой оксалатов. Однако употребление ксилита в дозе более 50 г в день может вызвать понос. Поэтому комитет считает нецелесообразным устанавливать среднесуточную дозу потребления (Average Daily Intake) для этого полиола, но не возражает против применения ограничений, связанных с его послабляющим действием.
Маннит
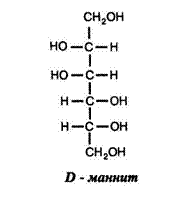 Маннит является шестиатомным спиртом и обнаружен впервые Проутсом в так называемой манне. Это название дано лишайнику Lecanora (Aspicillia) escubenta и другим близким видам, которые встречаются в степях южных стран, имеют вид небольших бугорчатых комочков, неприкрепленных к почве, легко переносятся на большие расстояния ветром. При необходимости они применяются в пищу. Манной также называют засохший сок некоторых растений, который скапливается в месте укусов насекомых или надрезов на коре. Особенно много манны на ветвях ясеня манного и ясеня круглолистного. Богаты манной также верблюжьи колючки. Было установлено, что в состав манны, наряду с другими сахарами, входит маннит, содержание которого зависит от исходного продукта. Так, например, в манне из ясеня манного и ясеня круглолистного содержание маннита достигает 40-50 %. Наибольшее его количество обнаружено в австралийской манне из растения Myoporum pla-ticapum — до 90 %. Кроме манны, маннит обнаружен в листьях, стеблях, корнях и клубнях ятрышника, сельдерея, цветной капусты, турецких бобов, сирени, жасмина, в ржаном хлебе, высушенных грибах и некоторых морских водорослях. Наиболее распространенной изомерной формой является D-маннит.
Маннит является шестиатомным спиртом и обнаружен впервые Проутсом в так называемой манне. Это название дано лишайнику Lecanora (Aspicillia) escubenta и другим близким видам, которые встречаются в степях южных стран, имеют вид небольших бугорчатых комочков, неприкрепленных к почве, легко переносятся на большие расстояния ветром. При необходимости они применяются в пищу. Манной также называют засохший сок некоторых растений, который скапливается в месте укусов насекомых или надрезов на коре. Особенно много манны на ветвях ясеня манного и ясеня круглолистного. Богаты манной также верблюжьи колючки. Было установлено, что в состав манны, наряду с другими сахарами, входит маннит, содержание которого зависит от исходного продукта. Так, например, в манне из ясеня манного и ясеня круглолистного содержание маннита достигает 40-50 %. Наибольшее его количество обнаружено в австралийской манне из растения Myoporum pla-ticapum — до 90 %. Кроме манны, маннит обнаружен в листьях, стеблях, корнях и клубнях ятрышника, сельдерея, цветной капусты, турецких бобов, сирени, жасмина, в ржаном хлебе, высушенных грибах и некоторых морских водорослях. Наиболее распространенной изомерной формой является D-маннит.
В природных условиях маннит синтезируется из других сахаров при помощи специфических бактерий: например, он легко образуется в соке спаржи при длительной экспозиции на холоде. В промышленности его получают из морских коричневых водорослей или каталитическим гидрированием сахарозы. При этом происходит ее инверсия с образованием глюкозы и фруктозы, восстанавливающихся соответственно в сорбит и маннит. Разработаны также методы химического синтеза маннита.
Калорийная ценность маннита ниже ксилита и составляет 8,5 кДж/г. Он не нашел применения как сахарозаменитель, так как его сладость по сравнению с сахарозой составляет 0,4-0,7. Благодаря специфическим свойствам, маннит используется в медицинской практике в качестве желчегонного и диуретического средства осмотического типа. Он оказывает дегидратаци-онное действие, выраженное влияние на водно-солевой обмен, а также детоксикационный эффект. Введенный внутривенно маннит значительно повышает осмотическое давление плазмы крови, что вызывает приток интерстициальной жидкости в сосудистое русло, увеличивает объем циркулирующей жидкости и снижает показатель гематокрита. Попадая в просвет проксимальных канальцев, он повышает осмотическое давление, что препятствует реабсорбции воды и увеличивает ее выведение (Л.В. Ленцер и соавт., 1967).
Маннит не токсичен, однако, не проникая в клетки, он может накапливаться в межклеточном пространстве и вызывать нарушение баланса электролитов (так называемую водную интоксикацию). Поэтому лечение маннитом рекомендуют проводить под контролем содержания натрия в плазме крови.
Основными показаниями для введения раствора маннита являются острая почечная недостаточность в результате шока, обширные массивные травмы, тяжелые ожоги, резкая гипотония и другие состояния, сопровождающиеся олиго- и анурией. Кроме того, абсолютными показаниями для его применения являются гемотрансфузионные осложнения и другие состояния, сопровождающиеся гемолизом. Он используется для предупреждения острой почечной недостаточности, при операциях с искусственным кровообращением, отеке мозга и других неотложных неврологических случаях ликворной гипертензии, операциях на головном мозге, при повышении внутриглазного давления, отравлениях и интоксикациях, а также для определения скорости клубочковой фильтрации. Благодаря свойству маннита оказывать раздражающее действие на слизистую оболочку двенадцатиперстной кишки, происходит выделение гормона холецистокинина, который вызывает сокращение желчного пузыря и оказывает желчегонный эффект.
Маннит также применяют для профилактики и лечения нарушений водно-солевого обмена, возникающих в результате избыточного введения жидкости при операциях с использованием экстракорпорального кровообращения с гемодилюцией. Его не рекомендуют вводить при сердечной недостаточности с выраженной внеклеточной гидратацией, повышенной кровоточивостью, внутричерепных гематомах, а также в случае органических изменений в почках. Обычно маннит вводят внутривенно капельно (Ф.В. Баллюзек и соавт., 1967). Суточная доза не должна превышать 140-180 г.
Комитет по продуктам питания ЕС не обнаружил противопоказаний для длительного применения маннита в качестве сахарозаменителя, без установления "среднесуточной дозы потребления". Однако его применение в этом качестве не нашло широкого распространения в силу низкой сладости по отношению к сахарозе.
Мальтитол
Мальтитол имеет приятный сладкий вкус, подобно сахару, и по интенсивности составляет примерно 90 % его сладости. Его производят путем гидрогенизации мальтозы, которую получают из крахмала. Как и другие полиолы, он не приобретает коричневого цвета и не карамелизируется, как сахар. В настоящее время его производят мощные компании Cerestar, Roquette, SPI Polyols Inc. и Towa Chemical Industry Co LTD. По сравнению с другими полиолами мальтитол оказывает незначительный "холодящий" эффект во рту. Его применяют не только как сахарозаменитель, но и как заменитель жира, в связи с его свойством придавать "сливочный вкус" пище (J. Lederer и соавт., 1974).
Практически под названием "мальтитол" рассматриваются продукты, полученные путем ферментативного гидролиза крахмала с последующей каталитической гидрогенизацией для связывания свободных альдегидных групп. Содержание собственно мальтитола в этих продуктах колеблется от 50 до 95%.
Было доказано, что мальтитол не подвергается метаболизму бактериями ротовой полости, которые, расщепляя сахар или крахмал, выделяют кислоты, способствующие нарушению зубной эмали и развитию кариеса.
Мальтитол медленно абсорбируется в кишечнике, поэтому подъем глюкозы и инсулина в крови происходит более редуцированно по сравнению с приемом сахарозы. В организме он медленно, но полностью разлагается на глюкозу и сорбит, особенно кишечной флорой. Кроме того, учитывая, что энергетическая ценность мальтитола составляет 2,1 кал/г (сахара — 4,0 кал/г), он может применяться в диетах для снижения массы тела. Согласно положению FDA, действующему в США, продукты могут обозначаться как "снижающие калории", если они обеспечивают их уменьшение, по меньшей мере, на 25 %. Поэтому мальтитол соответствует такому обозначению. В ЕС, согласно Национальной маркировочной директиве, все полиолы, включая мальтитол, оцениваются по энергетической ценности в 2,4 кал/г.
Мальтитол является безопасным продуктом для здоровья и всеми регламентирующими органами США и Европы разрешен к применению без ограничений.
Учитывая, что, подобно другим полиолам, мальтитол может оказывать в больших дозах послабляющий эффект, его не рекомендуют применять более 100 г в день. Послабляющий эффект наблюдается и при более низких дозах (30-50 г в день).
Мальтитол разрешен к применению как вещество, обладающее не только свойством сахарозаменителя, но и другими качествами пищевых добавок (стабилизаторов, загустителей, наполнителей и др.). Он может применяться при изготовлении шоколада и шоколадных покрытий, так как, в отличие от других полиолов, имеет безводную, низкогигроскопическую стабильную кристаллическую форму с низкой точкой плавления.
Гидрогенизированный гидролизат крахмала
Это общее название объединяет следующие продукты: гидрогенизированный сироп глюкозы, сироп мальтитола, сироп сорбита. Впервые технология получения таких продуктов была разработана в 60-х годах в Швеции, путем частичного гидролиза кукурузного, пшеничного или картофельного крахмала и последующей гидрогенизации при высокой температуре и давлении. В зависимости от условий проведения технологического процесса, образуются конечные продукты с преимущественным содержанием мальтитола, сорбита и высокогидрогенизированных сахаридов (малтитритола и др).
Термин "гидрогенизированный гидролизат крахмала" может быть применим к любым полиолам, которые получают путем гидрогенизации сахаридных продуктов крахмального гидролиза. Однако на практике этот термин чаще применяется при описании группы полиолов, содержащих определенное количество гидрогенизированных олиго- и полисахаридов в дополнение к любым мономерным и димерным полиолам (сорбит/маннит или мальтит). Продукты, не содержащие специфических полиолов как преимущественного компонента, обозначаются общим термином "гидрогенизированный гидролизат крахмала". Он имеет приятный сладкий вкус, интенсивность которого составляет от 40 до 90 % сладости сахарозы, и хорошо сочетается в смесях с другими сахарозаменителями, маскируя" горький привкус некоторых из них.
Каковы положительные свойства гидрогенизированного гидролизата крахмала? Он медленно всасывается в пищеварительном тракте и медленно расщепляется до простых полиолов. Поэтому гидролизованный гидрогенизированный крахмал вызывает подъем уровня глюкозы и инсулина крови в значительно меньшей степени, чем сахароза. Это качество позволяет рекомендовать его больным сахарным диабетом, однако с обязательным учетом изменения гликемического профиля.
Кроме того, полиолы, входящие в гидролизат крахмала, резистентны к воздействию микроорганизмов ротовой полости и не повреждают зубную эмаль. В многочисленных исследованиях была доказана безвредность этого продукта для организма животных и человека. Этот сахарозаменитель относится к продуктам со сниженной калорийностью. Его энергетическая ценность не превышает 3 кал/г (калорийность сахара — 4 кал/г). Как уже отмечалось, согласно утвержденному положению ЕС, все полиолы, включая и "гидрогенизированный гидролизат крахмала", имеют калорийность, равную 2,4 кал/г.
В настоящее время этот сладкий продукт применяется во многих странах при изготовлении различных кондитерских изделий. Установлено, что он не только придает пище сладкий вкус, но также улучшает текстуру продукта, ингибирует кристаллизацию, снижает "пригорание" при выпечке, повышает его стабильность.
Лактитол
Рассматриваемый сахарозаменитель обратил на себя внимание своей стабильностью, растворимостью и сладостью. Лактитол был открыт в 1920 г., а впервые использован в качестве пищевой добавки в 1980 г. Интенсивность его сладкого вкуса составляет 40 % сахарозы.
В отличие от молочного сахара (лактозы), этот полиол не гидролизуется лактазой и плохо всасывается в тонкой кишке. Он метаболизируется бактериями в толстой кишке, превращаясь в биомассу, органические кислоты, двуокись углерода и водород. В дальнейшем органические кислоты усваиваются организмом и обеспечивают энергетическую ценность, равную 2 кал/г. Суммарная энергетическая ценность лактитола равна 2,4-2,6 кал/г (в отличие от углеводов — 4 кал/г). Лактитол имеет чистый сладкий вкус без послевкусия, не гигроскопичен, стабилен к действию кислот и щелочей, хорошо сочетается с интенсивными сахарозаменителями. Пища, приготовленная с использованием лактитола, не вызывает повышения уровня глюкозы и инсулина в крови, поэтому может применяться больными сахарным диабетом с учетом энергетической ценности. Этот сахарозаменитель не вызывает кариеса.
В 1984 г. Научный комитет по пищевым продуктам ЕС установил ежедневную дозу полиолов, включая лактитол, равную 20 г в день. В дальнейшем эти ограничения были отменены. Доказано, что лактитол относится к безопасным продуктам и его ежедневная доза не ограничивается. Научный комитет по пищевым продуктам ЕС считает нецелесообразным вводить "среднесуточную дозу потребления" для лактитола, однако считает необходимым учитывать его свойство оказывать диа-рейный эффект в дозе 50 г в день и выше. В настоящее время лактитол разрешен к применению также в Канаде, Японии и Израиле. С 1993 г. он разрешен к применению в виде пищевой добавки в США.
Эритритол
Сахарозаменитель эритритол употреблялся людьми на протяжении тысячелетий. Он входит в состав некоторых фруктов (сливы, дыня, виноград), грибов и продуктов, подвергнутых ферментации (вино, соевый соус). Эритритол относится к полиолам и с 1990 г. применяется в качестве подсластителя при изготовлении некоторых видов пищи и напитков. Этот сахарозаменитель — белый порошок с чистым сладким вкусом, подобным сахарозе, по интенсивности равен 70 % ее сладости. Как и другие полиолы, он не вызывает кариеса и безопасен для больных сахарным диабетом, не оказывая влияния на подъем глюкозы и инсулина в крови. Однако в отличие от других полиолов, он обладает очень низкой энергетической ценностью (0,2 кал/г), которая составляет примерно 7-13 % их калорийности и около 5 % калорийности сахарозы.
Так как эритритол быстро абсорбируется в тонкой кишке и быстро выводится из организма с мочой (более 90 %) — в течение 24 ч, послабляющий побочный эффект, иногда возникающий при избыточном потреблении полиолов, становится маловероятным при употреблении пищи, в состав которой входит эритритол. Учитывая, что только около 5 % эритритола достигает толстой кишки, где он подвергается метаболизму под действием кишечных бактерий, газообразование происходит в незначительной степени.
С 1997 г. эритритол разрешен к употреблению в США, а с 1990 г. применяется в Японии как пищевая добавка ко многим японским блюдам. Эритритол является одним из наилучших са-харозаменителей, применяемых в диетотерапии, направленной на снижение массы тела. Напомним, что, согласно принятым положениям, к таким продуктам относятся вещества, способствующие снижению энергетической ценности пищи на 25 %.
При введении эритритола крысам со стрептозотоциновым диабетом в дозах 100, 200 и 400 мг/кг массы в течение 10 дней, наблюдалось значительное снижение концентрации глюкозы в крови, печени и почках, а также уровня 5-гидроксиметилфур-фурола, как индикатора оксидативного стресса. Кроме того, обнаружено дозозависимое снижение продуктов взаимодействия с тиобарбитуровой кислотой в сыворотке и митохондриях, печени и почках. Авторы сделали заключение, что эритритол оказывает положительное влияние на углеводный обмен и нормализует показатели оксидативного стресса (Т. Yokozawa и соавт., 2002).
Клинические исследования показали, что ежедневное потребление эритритола в дозе 1 г/кг массы тела взрослых людей отлично переносится по сравнению с пищей, содержащей сахарозу. Он хорошо сочетается с низкокалорийными сахарозаменителями, такими, как аспартам и ацесульфам К, что позволяет повысить интенсивность сладкого вкуса при снижении количества входящих компонентов. Кроме того, добавление эритритола к другим сахарозаменителям позволяет избавиться от горького привкуса, присущего некоторым сладким веществам.
Изомальт
Этот сладкий продукт был получен в 1960 г. из сахара. Он является смесью двух дисахаридных спиртов — глюкозоманнитола и глюкозосорбитола. Обычно этот сахарозаменитель получают в две стадии: сначала нарушают связь между глюкозой и фруктозой в молекуле сахарозы, а затем присоединяют два атома водорода к кислороду во фруктозной части дисаха-рида (рис.). При этом примерно половина фруктозной части природного дисахарида превращается в маннит, а другая половина — в сорбит. Поэтому изомальт содержит два дисахаридных спирта. Описанные молекулярные изменения делают структуру изомальта более стабильной к химическому и ферментативному воздействию. Он представляет собой белые кристаллы без запаха, стоек к температурному влиянию, не теряет своих свойств при кипячении и выпечке. Изомальт абсорбирует воду в незначительных количествах, что положительно сказывается на хранении продуктов, его содержащих. Он не разрушается в пище, не растворяется во рту и не имеет "холодящего" послевкусия, в отличие от других полиолов.
Сладость изомальта зависит от концентрации, температуры и особенностей продукта, в котором он используется. При отдельном применении проявляет от 45 до 65 % сладости сахарозы. Поэтому для интенсификации сладкого вкуса изомальт часто используют в комбинации с интенсивными подсластителями. Кроме того, он маскирует горьковатый привкус некоторых из них.
Благодаря своим специфическим свойствам изомальт, как и другие полиолы, усваивается в желудочно-кишечном тракте в незначительном количестве, а неусвоившаяся часть метаболи-зируется кишечными бактериями. Это является нормальным физиологическим процессом, который у отдельных людей может вызывать размягчение кала и увеличение газообразования, подобно пище с высоким содержанием пищевых волокон. Но даже у чувствительных лиц не возникает проблем, если они начинают употребление изомальта в небольших дозах, а затем постепенно их увеличивают.
Положительным свойством изомальта является его низкая энергетическая ценность — 2 кал/г. Поэтому его рекомендуют применять для лечения больных с излишней массой тела. Кроме того, известно, что полиолы вызывают значительно более низкий гликемический ответ, чем сахароза или другие углеводы, и это — основное преимущество использования изомальта в диетическом питании больных сахарным диабетом. В многочисленных исследованиях доказано, что прием изомальта незначительно влияет на уровень глюкозы и инсулина у здоровых людей и больных диабетом 1-го и 2-го типа (G. Siebert и соавт., 1975; W. Bachmann и соавт., 1984; D. Thiebaud и соавт., 1984; М. Drost и соавт., 1980).
|
Глюкозо-фруктоза Глюкозо-маннитол и глюкозо-сорбитол 2-я стадия - присоединение двух атомов водорода к кислороду во фруктозной части дисахарида Рис. Схема получения изомальта |
Установлено, что этот сахарозаменитель не подвергается воздействию кислообразующих бактерий ротовой полости и тем самым предотвращает развитие кариеса. Наоборот, повышая саливацию, он снижает кислотность и увеличивает содержание кальция в поверхностной части зуба, что способствует восстановлению зубной эмали. Если пищевой продукт не снижает рН ротовой полости ниже 5,7 в течение 30 мин после его приема, то он может, согласно положению FDA, применяться с обозначением "не вызывает кариеса". Такое обозначение имеют продукты, содержащие изомальт. Он признан безопасным продуктом и получил разрешение на использование в США с 1990 г. Объединенный комитет экспертов по пищевым добавкам ВОЗ также признал его безвредность и одобрил его ежедневное употребление без ограничений. В настоящее время изомальт используется более чем в 40 странах мира.
Глицерин (масляный сахар)
В 1779 г. химик и фармацевт Карл Вильгельм Шееле при омылении оливкового масла окисью свинца (метод получения свинцового пластыря) выделил неизвестное вещество сладкого вкуса, которое затем, обрабатывая азотной кислотой, можно было превратить в щавелевую кислоту. Он назвал это вещество "масляным сахаром". В дальнейшем Шееле обнаружил его в коровьем масле и свином жире. Оно отличалось от сахара тем, что не кристаллизовалось и не подвергалось брожению. Повторно это вещество было открыто в 1813 г. Шеврелем, который дал ему название "глицерин" (glycerinum от греческого "glykeros", что означает сладкий). Он показал, что все жиры являются соединениями глицерина с кислыми веществами. В 1854 г. Вюрц установил, что глицерин — трехатомный спирт, а в 1857 г. получил его методом, применяемым при синтезе гликолей. Правильную структурную формулу "масляного сахара" впервые определил Бутлеров в 1859 г.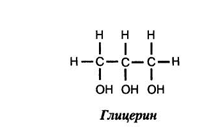
Глицерин является достаточно стойким соединением при нагревании, замораживании, а также при смешивании с водой и многими органическими растворителями. Он обладает высокой гигроскопичностью и может поглощать до 40 % воды по отношению к первоначальному объему. При обезвоживании глицерина образуется акролеин — вещество с неприятным раздражающим запахом, напоминающим кухонный чад при жарении жирных продуктов.
В организме глицерин образуется как при распаде жиров (триглицеридов) и глицерофосфолипидов, так и при анаэробном распаде глюкозы, являясь, таким образом, связывающим звеном жирового и углеводного обмена.
В силу слабовыраженного сладкого специфического вкуса глицерин не нашел широкого применения в пищевой промышленности. Его применяют для подслащивания вин, ликеров и лимонадов. Гигроскопические свойства глицерина используют в текстильном производстве, а также в полиграфии для приготовления невысыхающих красок.
В фармации он входит в состав мазей, паст и лосьонов для смягчения кожи. Растворы глицерина применялись в медицинской практике как противоотечное средство. Учитывая, что глицерин при проникновении в клетку ослабляет эффект кристаллизации воды, его используют в качестве криопротек-тора для сохранения живых тканей в условиях низких температур.
Более широкое применение получило производное глицерина — нитроглицерин, который известен как кардиологический препарат, а также как взрывчатое вещество при производстве динамита.
Синтетические сахарозаменители
Сахарин
История использования сахарина начинается с 1879 г., когда два американских химика из Университета Джона Гопкинса Фахльберг и Ремсен случайно его синтезировали. Сначала он использовался как антисептик и консервант, тормозящий ферментацию пищи Однако вскоре были обнаружены его сладкие свойства, и он на долгие годы вошел в качестве сахарозаменителя в питание людей.
Сахарин является наистарейшим синтетическим сахарозаменителем. Его сладость превышает таковую сахарозы в 300 раз, а сладкий вкус может ощущаться в разведении 1 часть на 100 000. Однако в концентрации, превышающей 0,1 %, его вкус ощущается как горький.
Франция была первой страной, которая в 1880 г. запретила употребление, импорт и производство сахарина как вредного продукта. Аналогичные решения приняли и другие европейские страны.
Начиная с 1884 г., в США Фахльберг наладил производство сахарина. В это время доктор H.Wiley, руководитель отделения химии Отдела сельского хозяйства США попытался приостановить употребление этого соединения в стране. Он сформировал "токсикологическую группу" из 12 волонтеров для оценки отдельных ингредиентов пищи, некоторые из них в том числе и сахарин, были признаны токсическими. После проведения исследований H.Wiley рекомендовал президенту Теодору Рузвельту запретить использование сахарина, так как он "высоко вредный для здоровья". Однако президент раздраженно ответил: "Вы говорите, он вреден для здоровья? Почему же доктор Рикси дает мне его каждый день? Любой, кто говорит, что сахарин вреден для здоровья, является идиотом" (F.C. Morris, 1980). Для того чтобы получить научное подтверждение опасности сахарина, Рузвельт в 1907 г. сформировал комиссию для исследования его влияния на питание и здоровье людей. При этом он возглавил Совет научных экспертов. После рассмотрения имеющихся данных Совет признал возможным применение сахарина как пищевой добавки (М. Allen, 1973).
В Европе заметное повышение потребления сахарина стало наблюдаться в течение второй мировой войны в связи с недостатком сахара. Однако его применение, особенно при изготовлении пищи, ограничивалось горьким послевкусием и лабильностью к температуре (M.F. Cranmer, 1980).
Сахарин является имидом о-сульфобензойной кислоты и представляет собой бесцветные кристаллы без запаха, хорошо растворимые в горячей (1:28) и плохо — в холодной воде. В продажу обычно поступает натриевая соль сахарина, которая лучше растворяется в воде и была известна ранее под названием " кристаллоза". При кипячении в водном растворе сахарин образует о-сульфамидбензойную кислоту, обладающую не сладким, а горьким вкусом.
Поступая в организм, сахарин всасывается не полностью. Около 6-8 % введенного вещества выделяется с калом, а около 90 % —с мочой в неизмененном виде. Период полувыведения составляет 20-30 мин. Примерно 1 % сахарина метаболизируется в организме до о-сульфамидбензойной кислоты и о-сульфобензойной. После введения он накапливается больше всего в мочевом пузыре, в меньшей степени — в почках, печени, легких и селезенке. Сахарин проникает через плацентарный барьер и накапливается в органах плода, выделяясь более медленно, чем из организма матери.
В течение длительного периода применения сахарина были отмечены лишь единичные побочные явления — он повышал диурез (что заставило ограничить дозу до 0,01-0,05 г в день), в редких случаях наблюдалась фотосенсибилизация. Полулетальная доза сахарина для мышей и крыс составляет 175 г/кг.
Однако в 70-х годах прошлого столетия возникли сомнения относительно безвредности сахарина, так как было обнаружено, что его употребление может способствовать развитию рака мочевого пузыря у экспериментальных животных. Так, G. Bryan (1970) обнаружил рак мочевого пузыря при инстилляции или введении сахарина в корм крысам. Затем эти данные подтвердили и другие исследователи (G.R. Howe и соавт., 1977; R.N. Hoover, P.H. Strasser 1980; A.S. Morrison, J.E. Buring, 1980). Показано, что в больших дозах сахарин также приводит к развитию опухолей у животных второго поколения. Кроме того, доказано его коканцерогенное действие, когда он способствовал ускоренному развитию опухолей мочевого пузыря у крыс при введении нитрозомочевины. Злокачественное перерождение наблюдалось, если доза сахарина составляла от 1 до 10 % общей массы корма, а при внутрибрюшинном введении — от 50 до 200 мг/кг. Некоторые исследователи при внутрибрюшинном введении сахарина наблюдали повышение содержания ДНК в печени и почках, что может являться следствием разрыва спирали молекулы (R.M. Hicks и соавт., 1973).
Безопасность сахарина оценивал Объединенный комитет экспертов FAO/BO3 по пищевым добавкам на 11-й и 18-й сессиях в 1968 и 1974 гг. соответственно. В то время были установлены уровни безусловно допустимого суточного потребления сахарина (ДСП) — до 5 мг на 1 кг массы тела — и условно допустимого потребления (в диетических целях) — 15 мг на 1 кг массы тела. На совещании в Женеве в апреле 1977 г. Объединенный комитет экспертов рассмотрел данные трех исследований канцерогенности сахарина, в которых наблюдалось значительное повышение частоты возникновения опухолей мочевого пузыря у поколения Fj крыс-самцов, пищевой рацион которых содержал 5 % или более сахарина. В этих исследованиях, отличавшихся от предыдущих долгосрочных экспериментов, животные получали сахарин с молоком матери, а затем в течение всей жизни (О.М. Jensen, С. Kamby, 1982). Гипотеза о том, что о-толуолсульфонамид — основная примесь сахарина — может быть канцерогеном, была исключена, поскольку это соединение само по себе не вызывало опухолей мочевого пузыря у крыс (D.L. Arnold и соавт., 1980). Кроме того, опухоли мочевого пузыря наблюдались и при использовании сахарина, не содержащего этой примеси. Сахарин не вызывал опухолей мочевого пузыря во многих других стандартных долгосрочных исследованиях, в ходе которых этот продукт давали нескольким видам животных. Изучение мутагенности сахарина дало как положительные, так и отрицательные результаты. Эта несогласованность объяснялась присутствием какой-то еще не идентифицированной примеси, являющейся сильным канцерогеном. Возможно, что сахарин действует как вещество, способствующее развитию опухолей (коканцероген).
Принимая во внимание озабоченность по поводу возможного вредного действия сахарина на человека, Объединенный комитет экспертов заменил ранее установленное безусловное для человека ДСП 5 мг/кг на 2,5 мг/кг и отменил прежнее условное ДСП 15 мг/кг.
Целесообразно описать подробные исследования канцерогенности сахарина, которые были проведены в Институте питания АМН СССР на крысах и мышах (А.С. Ивашкина, Г.Н. Архипов, 1980). При этом изучался основной путь введения сахарина в организм животных — с кормом в дозе 2500 мг/кг (1/10 ЬД5о). Кроме того, сахарозаменитель в парафино-сахариновом депо инокулировали под кожу крыс и в 13 Уо ацетоновом растворе апплицировали на кожу мышей. Также изучали действие сахарина, вводимого с кормом, на развитие индуцированных бензпиреном кожных опухолей у мышей и на процесс спонтанного канцерогенеза.
В опыте на крысах при введении препарата с кормом на фоне контрольных животных, содержащихся на стандартном рационе, канцерогенность сахарина была очевидной. У крыс, получавших сахарин, возникли опухоли в тех органах и тканях, в которых у контрольных животных они не наблюдались совсем или наблюдались в единичных случаях. Так, опухоли развились в мочевом пузыре и предстательной железе у 7 подопытных животных, тогда как у контрольных крыс опухоли этой локализации отсутствовали. У подопытных животных развилось также 12 опухолей подкожной клетчатки, в контроле — только 1 опухоль. Суммарный выход опухолей у подопытных животных почти втрое (31 животное с опухолями) превышал этот показатель в контроле (опухоли у 11 крыс). В других опытах (инокуляция под кожу, кожная аппликация, сочетание с бензпиреном) не было выявлено ни бластомогенной активности, ни способности сахарина модифицировать опухолевый процесс. На основании проведенных исследований авторы сделали вывод, что сахарин обладает канцерогенной активностью и не может быть рекомендован в качестве пищевой добавки.
В отличие от экспериментальных исследований, подтверждающих канцерогенные свойства сахарина, при изучении его влияния на людей получены разноречивые результаты. В основном проводились исследования, направленные на освещение двух типов.
1. Насколько часто люди, у которых обнаружены опухоли мочеполовой системы, употребляли сахарин.
2. Как часто возникают опухоли мочевого пузыря среди популяции людей, применяющих различные продукты.
В 1980 г. опубликованы данные исследований (592 больных раком нижнего отдела мочевыводящих путей и 536 здоровых лиц), в которых установлено, что для людей, регулярно потреблявших сахарин в течение десяти лет, опасность заболеть раком мочевого пузыря была на 10 % выше, чем у людей, не употреблявших сахарина (New Scientiste, 1980, 85, 1198, 816). Эти результаты заставляют задуматься, несмотря на то, что такая степень риска является невысокой и не возрастает при увеличении количества потребляемого сахарина (New England J. Med., V. 302, P. 538).
Ранее эпидемиологи Американского фонда здоровья не выявили увеличения риска заболевания раком мочевого пузыря для лиц, потребляющих сахарин. Кроме того, в других эпидемиологических исследованиях, проведенных среди больных сахарным диабетом, также не обнаружили повышенного риска в отношении возникновения рака мочевого пузыря. Однако эти исследования были несовершенными (недостаточные масштабы выборки, неоднородность изучаемых групп населения, неизбежные статистические ограничения). В то же время, обе группы исследователей пришли к заключению, что нецелесообразно исключать сахарин из числа веществ, обладающих потенциальным канцерогенным эффектом, поскольку для проявления его отрицательного действия, возможно, необходим значительный промежуток времени, например 40-50 лет.
Учитывая, что в пище сахарин употребляется в дозах, намного меньших (в 50-100 раз), чем те, которые использовали в экспериментах на животных, а также то, что не были получены убедительные доказательства как отсутствия его канцерогенного эффекта и абсолютной безопасности, так и способности вызывать развитие опухолей у людей, во многих странах он применяется с определенными ограничениями. Так, в СССР, согласно ГОСТу, его количество в готовом продукте не должно было превышать 0,015-0,020 % и потребителя необходимо было поставить в известность о том, что отпускаемый продукт приготовлен на сахарине (указание на этикетке). Отмечалось, что постоянное его применение нежелательно. При этом он ограниченно использовался в производстве некоторых диетических напитков, кондитерских и хлебобулочных изделий, а также особых зубных паст. Продукты с добавлением сахарина должны были относиться к категории диетических. Однако в настоящее время он употребляется редко. Сахарин если и применяется, то добавляется в незначительных количествах к другим заменителям сахара и редко — самостоятельно. В некоторых странах Западной Европы на столах рядом с сахаром находятся пакетики, содержащие смесь 40 мг одного из безопасных сахарозаменителей и 4 мг сахарина. Сочетание двух сахарозаменителей позволяет усилить сладкий вкус, значительно снизить их дозу и неприятный привкус.
Учитывая, что сахарин практически не метаболизируется в организме, применение его было противопоказано при почечной недостаточности и склонности к образованию камней в почках и мочевом пузыре (более 90 % поступившего в организм сахарина выводится в неизмененном виде через почки). Поэтому его нельзя безоговорочно рекомендовать больным сахарным диабетом, у которых одним из осложнений заболевания часто является почечная недостаточность.
Институт питания РАМН также не рекомендовал применять сахарин в питании беременных женщин и детей, поэтому данный продукт нельзя регистрировать как "подсластитель для детских лекарственных форм".
Благодаря своей высокой сладости он нашел применение также в качестве диагностического средства при исследовании транспортной функции мерцательного эпителия. Разработчики этого метода предлагают помещать крупинку натриевой соли сахарина диаметром 0,6 мм на верхнюю поверхность нижней носовой раковины, отступя 5 мм от места прикрепления ее переднего конца, при этом время появления вкусового ощущения у здоровых лиц равняется в среднем 14 мин 55 с. Исследователи дают высокую оценку этому тесту и рекомендуют использовать его не только для диагностики синдромов цилиарной дискинезии, но и дифференциации различных форм ринита. Данный метод оказался наиболее простым и таким же информативным, как регистрация движения радиоактивных частиц, что позволило рекомендовать его для использования в широкой клинической практике. Единственным недостатком пробы является невозможность ее применения у детей младшего возраста (Г.В. Лавренова, 1987).
Возвращаясь к теме о безвредности сахарина, необходимо отметить, что, по мнению специалистов, ни одно вещество не может считаться безопасным для человека, если в опытах оно оказалось канцерогенным или бластомогенным (вызывающим рак или другие опухоли) для какого-либо вида животных, причем в любой дозе при одном или различных путях введения. Поэтому после того как Канадский отдел здравоохранения сообщил о том, что рак мочевого пузыря был обнаружен во второй генерации крыс-самцов, конгресс США объявил мораторий на его использование до получения дополнительных данных о его безопасности. В апреле 1983 г. президент Р. Рейган подписал это решение и определил термин моратория до 22 апреля 1985 г. Были проведены дополнительные исследования, в одном из которых анализировались гистологические изменения в срезах мочевого пузыря людей, у которых зафиксированы клетки с нетипичными ядрами. Всего было исследовано 6503 среза от 282 пациентов. При этом не было обнаружено взаимосвязи между изменениями эпителия мочевого пузыря и употреблением искусственных сахарозаменителей. Эти работы были опубликованы Аурбахом и Горфинкелем в 1989 г. Кроме того, опубликованы также результаты еще одного исследования, проведенного группой врачей, которые ранее, в 1977 г., обнаружили повышение риска от употребления сахарина у мужчин (фактор вероятности 1,6), но не у женщин (проанализированы данные 480 мужчин и 152 женщин). В 1988 г. эта группа исследователей представила в печать результаты анализа 826 случаев гистологически подтвержденного рака мочевого пузыря. При этом относительный риск его развития, по мнению авторов, не имел связи с употреблением синтетических сахарозаменителей, включая сахарин.
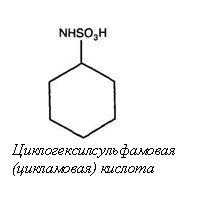 После проведенного широкомасштабного эпидемиологического исследования причин возникновения рака мочевого пузыря в Канаде один из руководителей этих работ, доктор С. Миллер, высказал заключение, что риск возникновения данного заболевания при употреблении сахарина в 2 раза меньше, чем "при посещении доктора или употреблении кофе. Риск развития рака мочевого пузыря почти в 10 раз выше у женщин, курящих сигареты, и в 25 раз выше, если при этом также употреблять кофе" (G.R. Nujem и соавт., 1982; S.A. Miller, V.P. Frattal, 1989; R.W. Morgan, M.G.Jain, 1974).
После проведенного широкомасштабного эпидемиологического исследования причин возникновения рака мочевого пузыря в Канаде один из руководителей этих работ, доктор С. Миллер, высказал заключение, что риск возникновения данного заболевания при употреблении сахарина в 2 раза меньше, чем "при посещении доктора или употреблении кофе. Риск развития рака мочевого пузыря почти в 10 раз выше у женщин, курящих сигареты, и в 25 раз выше, если при этом также употреблять кофе" (G.R. Nujem и соавт., 1982; S.A. Miller, V.P. Frattal, 1989; R.W. Morgan, M.G.Jain, 1974).
Удалось также определить наиболее вероятные причины канцерогенного действия высоких доз сахарина у крыс. Установлено, что гиперплазия и стимуляция активности эпителия мочевого пузыря наблюдается при введении сахарина выше 5 % в диете на фоне повышения концентрации натрия и рН. Эта реакция организма является неспецифической, но именно она, как считают исследователи, ответственна за негативные эффекты сахарозаменителя. Известно, что высокие концентрации других неорганических ионов в диете стимулируют канцерогенез в мочевом пузыре в аналогичных условиях. Поэтому органическая часть молекулы натриевой соли сахарина, по мнению экспертов, в данном процессе не принимает участия.
Исходя из противоречивости всех данных, полученных за весь период применения сахарина, главная регламентирующая организация США, Администрация по пищевым продуктам и лекарствам (FDA), в 1993 г. разработала положение о применении этого сахарозаменителя, обязав производителей на упаковке продуктов делать следующую надпись: "Использование этого продукта может быть опасным для вашего здоровья. Этот продукт содержит сахарин, который, как установлено, может вызывать рак у лабораторных животных". С такой надписью американская компания "Sweet'n Low" выпускала сахарин в продажу, пока не заменила его на другие, более безопасные вещества (рис.).
 В Западной Европе было принято несколько другое решение. В 1993 г. Объединенный экспертный комитет по пищевым добавкам FAO/BO3 в 41-м докладе признал недостаточными результаты проведенных ранее исследований для утверждения о канцерогенной опасности сахарина для человека. При этом комитет установил дозу ежедневного применения сахарина 0-5 мг/кг вместо принятой ранее 0-2,5 мг/кг, исходя из максимальной дозы, не вызывающей токсических явлений при назначении крысам в двух поколениях и равной 500 мг/кг с учетом фактора безопасности, равным 100. Особо подчеркивалось, что сахарин может применяться только в диетическом питании.
В Западной Европе было принято несколько другое решение. В 1993 г. Объединенный экспертный комитет по пищевым добавкам FAO/BO3 в 41-м докладе признал недостаточными результаты проведенных ранее исследований для утверждения о канцерогенной опасности сахарина для человека. При этом комитет установил дозу ежедневного применения сахарина 0-5 мг/кг вместо принятой ранее 0-2,5 мг/кг, исходя из максимальной дозы, не вызывающей токсических явлений при назначении крысам в двух поколениях и равной 500 мг/кг с учетом фактора безопасности, равным 100. Особо подчеркивалось, что сахарин может применяться только в диетическом питании.
Следует отметить, что сахарин не является жизненно необходимым лекарственным средством, чтобы обсуждать возможности его применения при спорных вопросах его повышенной опасности для здоровья. Особенно это касается людей, живущих в неблагоприятной экологической среде. Сахарин без особого труда может быть заменен. Какой смысл использовать потенциально сомнительные пищевые добавки, когда есть безвредные? Поэтому в Фармакологическом комитете Украины было принято решение: учитывая неблагоприятную экологическую обстановку в Украине, не проводить регистрацию сахарина и продуктов, его содержащих (сукразид, сукравит и др.). Одновременно Ученый совет НИИ эндокринологии и обмена веществ АМН Украины не рекомендовал применение сахарина в качестве сахарозаменителя у больных сахарным диабетом. В тоже время, специалисты считают возможным его использование для широкого применения в смеси с другими безопасными сахарозаменителями в соотношении 40:4 (сахарозаменитель:сахарин) только в диетических продуктах как "добавку к пище", но не "пищевую добавку".
Цикламаты
Цикламатами называют натриевую соль и кальциевую соль циклогексилсульфамовой кислоты. Впервые их сладкие свойства обнаружены в 1937 г. Сведом в Иллинойском университете при изучении производных аминосульфокислот. Было замечено, что если цикламаты попадали на сигареты, последние приобретали сладкий вкус. Практическое их использование как сахарозаменителей началось в США с 1950 г. Вначале использовали натриевую соль, которая обладала более приятным сладким вкусом. Кальциевая соль имела незначительный горьковато-металлический привкус и нашла применение в консервной промышленности в силу ее более выраженной устойчивости к нагреванию. Кроме того, кальциевую соль рекомендуют лицам, которым противопоказано употребление натрия.
Натриевая соль цикламовой кислоты представляет собой белый кристаллический порошок, хорошо растворимый в воде (1:5). Водные растворы имеют нейтральную реакцию. Она в 30-50 раз слаще сахарозы и обладает более приятным сладким вкусом, чем сахарин. В присутствии органических кислот, например, во фруктовых соках, сила сладости по сравнению с сахаром повышается в 80 раз. Сладость растворов цикламата натрия возрастает до концентрации 1%, а в дальнейшем не изменяется. Цикламаты относятся к бескалорийным сахарозаменителями.
При исследовании обмена цикламата у экспериментальных животных и человека обнаружено, что коэффициент его абсорбции невелик (около 37%). По-видимому, этим можно объяснить послабляющее действие, которое большинство авторов связывают с повышением осмотического давления в кишечнике (Т. Friedmann и соавт., 1972; P.G. Branton и соавт., 1973; W. Low, 1979; К. Hwang, 1966). Резорбированный цикламат обнаруживается главным образом в крови, почках, печени, сердце и легких. Он переходит также в молоко и проникает через плацентарный барьер. Цикламат на 70 % связывается с белками крови, которые взаимодействуют с различными лекарствами, эндогенными гормонами, пищевыми продуктами и другими веществами. Установлено, что резорбция цикламата натрия угнетается фенобарбиталом, а повышается кофеином и лимонной кислотой. Большое влияние на резорбцию оказывает значение рН. Большая часть принятого цикламата (60 %) выделяется в неизмененном виде кишечником, около 35-40 % — почками. С помощью меченного изотопом цикламата было установлено, что он может проникать через плаценту. Его вводили внутривенно пяти женщинам, которые планировали прерывание беременности. После этого цикламат был обнаружен в крови и тканях плода (R.M. Pitkin и соавт., 1970).
Основными метаболитами, которые обнаруживаются в моче человека, являются циклогексиламин и дициклогексила-мин. В дальнейшем циклогексиламин в организме метаболизи-руется незначительно. Его обмен идет через гидроксилирован-ные кольца циклогексана (у крыс), путем дезаминирования (у человека), гидроксилирования кольца и дезаминирования (у морских свинок и кроликов). Степень превращения цикламата в циклогексиламин в организме человека составляет 30 % (A. Suenaga и соавт., 1983; A. Collings, 1989). Отмечалось, что при сахарном диабете обмен цикламата замедлен.
При одновременном приеме цикламата и антибиотиков выделение циклогексиламина уменьшается. Поэтому сделан вывод, что флора кишечника в основном отвечает за его метаболизм. В поддержку этого предположения свидетельствует еще тот факт, что у животных в гомогенате печени ни в одном из опытов не было обнаружено образования циклогексиламина. Другие вещества также оказывают влияние на метаболизм цикламата и соответственно на выделение его метаболитов. Так, фенилбутазон и фенобарбитал способствуют повышению выделения циклогексиламина, циклогексанола и циклогексанона, в то время как толбутамид только увеличивает выделение циклогексиламина.
Опыты на крысах показали, что LD50 для цикламата при пе-роральном введении равно 12 г/кг, при внутривенном — 3,5 г/кг. В хронических исследованиях токсичности цикламата на экспериментальных животных выявлено заметное влияние препарата на снижение их массы (Sabrim и соавт., 1969). Введение цикламата до или во время беременности уменьшает у крыс и морских свинок число имплантаций и величину плодов (J. Sultemeier, 1969). Рассасывание и число погибших плодов повышалось до отмены препарата. В опытах на мышах установлено, что сахарин, дульцин и цикламат оказывали тератогенное действие и были токсичны для эмбрионов (R. Tanaka, 1964). В последующем эти эксперименты были повторены и их результаты подтверждены, поэтому не рекомендуют применять цикламат во время беременности и в питании детей.
На основании опытов с крысами, которые ежедневно получали цикламат в дозе 20 мг/кг, сделан вывод об изменении поведения потомства, которое заключалось в гиперактивности. Этот факт послужил основанием для опроса 975 женщин со здоровым потомством и 247 женщин с детьми, имеющими замедленное развитие. При этом была установлена четкая и явная зависимость между потреблением цикламата и рождением детей с нарушением поведения. Но так как не были изучены и учтены другие сопутствующие факторы, как, например, возрастная структура матерей, полученные данные следует оценивать критически (D. Stone и соавт., 1970,1971).
В 1968 г. в опытах на животных установлено, что цикламат может вызывать повреждение печени и изменения в системе кроветворения (Е. Gottinger и соавт., 1968; А. Ассате, 1970). В 1969 г. в экспериментах на морских свинках отмечено, что повреждения паренхимы эпителия печени и почек, а также увеличение а-клеток поджелудочной железы наступают в результате гепатотоксического действия цикламата (К. Hagmuller и соавт., 1969). Определенный интерес представляют сообщения о том, что цикламат в опытах на животных уменьшал гипогликемическое действие толбутамида и хлорпропамида, что указывает на не вполне выясненное действие цикламата на поджелудочную железу (R. Lockwood, R. Dixon, 1969).
Наиболее важным из открытий явилась способность цикламата вызывать у опытных животных нарушение развития и рак мочевого пузыря (J. Price и соавт., 1970). В исследованиях на крысах была установлена прямая связь между введенной дозой циклогексиламина и процентом поломок хромосом в клетках спермы и костного мозга. Установлено, что кальциевая соль циклогексиламино-К-сульфоновой кислоты, подобно сахарину, стимулирует появление опухолей мочевого пузыря у крыс (до 60 %), которым предварительно вводили не канцерогенную метилнитрозомочевину. В опытах на хомяках, которые получали циклогексиламин в дозе 200 мг/кг, установлено статистически достоверное увеличение аберрации хромосом (G.T. de Went и соавт., 1975). Показано, что цикламаты индуцируют разрыв хромосом лейкоцитов и мононуклеаров человека (D. Stone и соавт., 1969).
На основании экспериментальных данных, приведенных выше, и в соответствии с предписанием о мерах предосторожности FDA издала распоряжение всем производителям и промышленным потребителям в США прекратить к концу 1969 г. производство и продажу цикламата. 18 октября 1969 г. ВОЗ опубликовала решение о запрещении продажи пищевых продуктов и напитков, содержащих цикламат, после 1 февраля 1970 г. (G.T. Bryan, E. Erturk, 1970; J. M. Price и соавт., 1970). Сходные запреты были опубликованы и в других странах: Франции (V. Borcaru, 1970), Швеции, Финляндии, Канаде, Японии, Великобритании и Польше. Подобный запрет был и в СССР.
Однако в дальнейшем эти решения начали пересматривать. Так, на Международном симпозиуме, посвященном сладким веществам, который состоялся в 1973 г. в Ганновере, данные о канцерогенном действии цикламата были признаны сомнительными на том основании, что в экспериментах применяли слишком высокие дозы, превышающие обычные в 500 раз, тогда как при меньших дозах препарата у крыс и мышей не выявили развития опухолей ни в мочевом пузыре, ни в других органах.
В 1984 г. Cancer Assessment Committee США и Администрация по лекарствам, а в 1985 г. Национальная Академия Наук США подтвердили безопасность цикламата. К такому же решению пришел в 2000 г. научный комитет по пищевым продуктам ЕС. Максимальное потребление цикламата, безопасное для здоровья, согласно рекомендациям Объединенного экспертного комитета по пищевым добавкам FAO/BO3 (с учетом 100-кратного коэффициента безопасности), в пересчете на цикламовую кислоту составляет 11 мг/кг, а согласно рекомендациям научного комитета по пищевым продуктам Европейской комиссии — 7 мг/кг.
В настоящее время употребление цикламата разрешено более чем в 50 странах мира, несмотря на то, что у некоторых специалистов отношение к нему продолжает оставаться настороженным.
Аспартам
Среди пептидов, обладающих сладким вкусом, наибольшее распространение получил метиловый эфир L-аспартил-Ь-фе-нилаланина. Он был открыт в 1965 г. при синтезе противоязвенных препаратов (R.H. Mazur, 1979). Аспартам является структурным аналогом С-концевых фрагментов и физиологически активных веществ пептидной природы, таких, как гаст-рин, холецистокинин и церулеин (L.R. Johnson, 1977; G.F. Rehfeld и соавт., 1980).
По степени сладости аспартам превосходит сахарозу в 200 раз и не имеет послевкусия. Интересно, что каждая из аминокислот, входящих в его состав, сладким вкусом не обладает.
При использовании аспартама снижается калорийность продуктов. Так, 1 г этого сахарозаменителя содержит 4 ккал (16,5 кДж), но принимаемая доза в 200 раз меньше, чем для сахарозы. Поэтому, например, калорийность чашки сладкого кофе уменьшается с 168 кДж при использовании сахарозы до 0,81 кДж после добавления аспартама. Однако надо учитывать, что он теряет сладость в сильнокислых и слабощелочных средах, например в чае с лимоном.
Как сахарозаменитель аспартам начал применяться в Англии и США с 1974 г. В настоящее время аспартам широко используется во всем мире. Так, его потребление в США в 1984 г. составило 1540 т, что эквивалентно 308 тыс. т сахара. Таблетки, содержащие аспартам, выпускаются под разными названиями: "Нейге Свит", "Санпа", "Кандерел", "Шугар Фри", "Сластилин" и др.
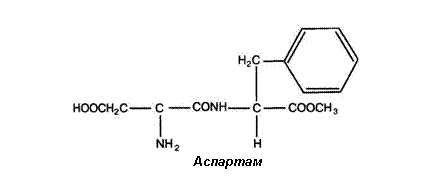 Доказано, что аспартам не влияет на секрецию инсулина и не обладает инсулинотропным действием (Н.В. Садовникова и соавт., 1984). При назначении добровольцам в дозе 80 мг он не вызывал повышения концентрации глюкозы и инсулина, в отличие от сахарозы. Не было также обнаружено изменения повышенного уровня жирных кислот после введения кофеина (Suzuki, 1984). Поэтому его без опасений можно применять при сахарном диабете и ожирении. В настоящее время его используют в качестве подсластителя при изготовлении джемов, пудингов, соков, жевательной резинки, некоторых видов хлеба, мороженого, йогурта, горячего шоколада (S. Colagiuri и соавт., 1989; D. Horwitz и соавт., 1988; В. Kanders, 1991; J. Nehrling и соавт., 1985).
Доказано, что аспартам не влияет на секрецию инсулина и не обладает инсулинотропным действием (Н.В. Садовникова и соавт., 1984). При назначении добровольцам в дозе 80 мг он не вызывал повышения концентрации глюкозы и инсулина, в отличие от сахарозы. Не было также обнаружено изменения повышенного уровня жирных кислот после введения кофеина (Suzuki, 1984). Поэтому его без опасений можно применять при сахарном диабете и ожирении. В настоящее время его используют в качестве подсластителя при изготовлении джемов, пудингов, соков, жевательной резинки, некоторых видов хлеба, мороженого, йогурта, горячего шоколада (S. Colagiuri и соавт., 1989; D. Horwitz и соавт., 1988; В. Kanders, 1991; J. Nehrling и соавт., 1985).
Аспартам усиливает сладкий вкус сахарозы, глюкозы, цикламатов и сахарина, снижая их дозу и подавляя неприятный привкус. Препятствием широкому внедрению аспартама в качестве подслащивающего агента служит его гидролиз в водной среде (при температуре 196 С0), приводящий к потере сладкого вкуса. При этом он превращается в безвкусный дикетопипе-разин. В коммерческих препаратах дикетопиперазин обнаруживается в количестве 1 % (Jost, 1982). Аспартам не теряет сладкого вкуса при температуре 150 °С в течение 45 мин, поэтому он не пригоден для изготовления пищевых продуктов, требующих термообработки, например, мороженого и кремов. Он практически не разлагается в сухих видах пищи, а в газированных напитках, хранящихся в течении 8 нед при температуре 20 °С, сохраняется 84-89 % сахарозаменителя, при 30 °С — 69 %. Процесс гидролиза можно затормозить, добавляя в раствор органические кислоты, или путем снижения температуры хранения. В сухом порошке растворимого кофе содержание аспартама за 260 дней снижается на 6-8 %.
При поступлении в желудочно-кишечный тракт аспартам расщепляется на составляющие его аминокислоты, обмен которых осуществляется обычным физиологическим путем (L. Filler, L. Stegink, 1989). Беспокойство вызвали сведения о том, что при расщеплении аспартама образуется метанол, который может оказывать токсическое действие на организм (L. Stegink и соавт., 1983). Однако в дальнейшем было доказано, что его содержание значительно меньше, чем в естественных продуктах питания. Так, в одной дозе аспартама (18-20 мг), которая соответствует 1 чайной ложке сахара, содержится 7,6 мг аспарагиновой кислоты, 9,5 мг фенилаланина и 1,9 мг метанола. В то же время, для сравнения, 100 г бананов содержат 134 мг аспарагиновой кислоты, 49 мг фенилаланина и 21 мг метанола. При суточной дозе аспартама 40 мг/кг массы тела образуется 4,4 мг метанола на 1 кг массы, тогда как отравление наступает при дозе метанола 200-500 мг/кг массы.
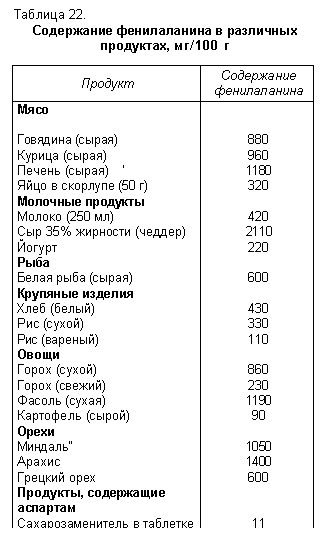 В 1994-1995 гг. появились сообщения о негативных явлениях, которые якобы могут возникать при использовании аспартама. Отмечалось, что наблюдались случаи развития парадоксального повышения аппетита, появления мигрени, изменения настроения, депрессии и других психических расстройств. Комитет по пищевым продуктам рассмотрел вопрос о возможном изменении поведения и настроения при введении аспартама и пришел к выводу, что те незначительные биохимические изменения, которые наблюдаются при одновременном его введении с глюкозой, не могут вызвать вышеуказанных нарушений (К.А. Lappier и соавт., 1988; Saravis и соавт., 1990; L. de Sonneville и соавт., 1991).
В 1994-1995 гг. появились сообщения о негативных явлениях, которые якобы могут возникать при использовании аспартама. Отмечалось, что наблюдались случаи развития парадоксального повышения аппетита, появления мигрени, изменения настроения, депрессии и других психических расстройств. Комитет по пищевым продуктам рассмотрел вопрос о возможном изменении поведения и настроения при введении аспартама и пришел к выводу, что те незначительные биохимические изменения, которые наблюдаются при одновременном его введении с глюкозой, не могут вызвать вышеуказанных нарушений (К.А. Lappier и соавт., 1988; Saravis и соавт., 1990; L. de Sonneville и соавт., 1991).
Обнаружено, что при введении аспартама в высокой дозе (200 мг/кг) вместе с глюкозой в моче крыс наблюдается повышение содержания фенилаланина в 2 раза и тирозина в 3 раза по сравнению с животными, которым вводили только глюкозу (R. Wurtman, 1983). Однако тщательные исследования не подтвердили эти наблюдения. Кроме того, было также рассмотрено влияние фенилаланина, который образуется при метаболизме аспартама, на состояние больных с резким генетическим заболеванием фенилкетонурией (R. Koch и соавт., 1976; K.L. Stegin и соавт., 1980), а также лиц с легкой формой этой болезни — гиперфенилаланинемией. При этом было установлено, что уровень фенилаланина в крови у обследованных людей повышался незначительно, так как содержание этой аминокислоты в ас-партаме существенно ниже, чем в некоторых пищевых продуктах (табл. 22). Кроме того, было показано, что аспартам не влияет на общее состояние беременных женщин, на течение родов и развитие плода. Не обнаружено также влияния на эмбрион у беременных женщин с фенилкетонурией. Для доказательства безвредности продуктов метаболизма аспартама изучались свойства основного его метаболита дике-топиперазина. На основании результатов биохимического анализа крови и мочи, а также гистологических исследований органов и тканей был сделан вывод об отсутствии токсического действия аспартама в сочетании с дикетопиперазином (Ishiu и соавт., 1981). Установлено, что доза дикетопиперазина, не вызывающая негативных явлений, равна 4000 мг/кг. Таким образом, безопасность аспартама была подтверждена в опытах на животных и на людях (при ежедневном применении в течение длительного времени в количествах, значительно превышающих 200 мг). FDA в очередной раз признала безопасность аспартама в ноябре 1986 г. В письме, отвергающем ограничения использования аспартама, отмечалось: "Данные и информация, подтверждающие безопасность аспартама, исчерпывающи. Похоже, ни один пищевой продукт не был так тщательно исследован на безопасность. Более того, решение агенства одобрить применение аспартама было принято, согласно самым высоким требованиям обычного процесса рассмотрения" (АМА, 1985).
3 ноября 1987 г. уполномоченный FDA Фрэнк Янг свидетельствовал перед сенатским комитетом, что "нет никаких медицинских или научных подтверждений, подрывающих нашу уверенность в безопасности аспартама. Эта уверенность базируется на годах изучения, анализе побочных явлений и научных исследований, включая исследования, поддерживаемые FDA".
27 июня 1996 г. FDA в 26-й раз одобрила употребление аспар-тама в качестве "подсластителя общего применения", подразумевая, что он может добавляться к любой пище, в которой индивидуальные особенности продуктов не препятствуют его использованию. Отмечалось, что безопасность применения аспартама подтверждается отсутствием серьезных побочных явлений, зарегистрированных за последние 23 года его применения. "Редкие соединения подверглись такому детальному тестированию, скрупулезным тщательным исследованиям, и эти исследования предоставляют общественности дополнительную уверенность в его безопасности".
Безопасность аспартама как пищевой добавки признана ВОЗ, Научным комитетом пищевой промышленности ЕС и соответствующими учреждениями более чем в 100 странах мира (А.В. Куликова и соавт., 1999). Он разрешен к применению в качестве пищевой добавки решением Европейского парламента (директива 94/35 ЕС) 30 июня 1994 г. Рекомендуемая ежедневная доза составляет 40 мг/кг.
В настоящее время аспартам является одним из наиболее часто употребляемых сахарозаменителей с приятным вкусом, который рекомендуется больным сахарным диабетом, беременным и кормящим женщинам, а также детям. Установлено, что употребление этого сахарозаменителя препятствует развитию кариеса. Однако, несмотря на официальное мнение, некоторые специалисты не рекомендуют его принимать беременным женщинам и детям до 7 лет. Он противопоказан при гомозиготной фенилке-тонурии, о чем необходимо указывать на этикетке.
Неотам
Сладкое вещество неотам состоит из двух аминокислот: L-аспарагиновой кислоты и L-фенилаланина, соединенных двумя органическими функциональными группами: метил-эфирной и неогексиловой. Этот сахарозаменитель примерно в 30 раз слаще аспартама. Он быстро метаболизируется и полностью выводится из организма путем естественных физиологических процессов. Неотам имеет чистый сладкий вкус, подобный сахарозе. Он может применяться при выпечке и варке, так как более стоек к температуре, чем аспартам.
Проведенные исследования продемонстрировали безвредность и безопасность неотама для организма. Эти данные были обобщены FDA, и в 1997 г. выдано разрешение на его применение в качестве столового сахарозаменителя.
Алитам
|
|
| Алитам |
К синтетическим пептидным веществам, обладающим чистым сладким вкусом, относится алитам, состоящий из аспара-гиновой кислоты, аланина и амида. Разработан он компанией "Pfizer" и выпускается под торговым названием "Aclame TM".
Этот сахарозаменитель в 2000 раз слаще сахара, обладает очень низкой калорийностью, которую можно не учитывать в диетическом питании, хорошо растворяется в воде, не разрушается при кипячении, безопасен для зубной эмали. Рекомендуется больным сахарным диабетом. Проведенные исследования подтвердили безопасность алитама для людей и животных. Он разрешен к применению в целом ряде стран и находится на рассмотрении в США и Научном комитете по пищевым продуктам ЕС.
Объединенный экспертный комитет по пищевым добавкам ВОЗ определил среднесуточную дозу потребления (ADI) в 1 мг/кг массы тела.
Ацесульфам К
|
Ацесульфам К |
В настоящее время во многих странах одним из наиболее популярных сахарозаменителей является ацесульфам К (ацесульфам калия), который был синтезирован в лабораториях немецкой компании "Hoechst A.G" в 1967 г. По химическому строению он является производным оксатиазина (3,4-дигидро-6-метил-1, 2, 3-окситиазин-4-ОН-2, 2-диоксид-калиевая соль) и известен под коммерческим названием "отизон". Ацесульфам К представляет собой белый кристаллический порошок без запаха, хорошо растворимый в воде (30 г на 100 мл при температуре 20 °С), обладает сладким вкусом, подобным глюкозе (без привкуса) и по интенсивности превышает сахарозу в 200 раз (Askar и соавт., 1981). После употребления в больших дозах он оставляет легкое послевкусие.
Этот сахарозаменитель стоек к высокой температуре (при рН 3,8 и температуре 40°С сохраняет стабильность в течение месяца), поэтому он может применяться при изготовлении горячей пищи, требующей кипячения, или кондитерских изделий, которые производятся при высокой температуре. Его растворы можно стерилизовать и пастеризовать. Ацесульфам К применяется в промышленности как самостоятельно, так и в комбинации с другими подсластителями при изготовлении холодных и горячих напитков, мороженого, фруктовых консервов, жевательной резинки, маринада для рыбных консервов и других продуктов, а также в фармацевтической промышленности для изготовления зубной пасты, таблеток и различных лекарственных форм. Он не повреждает зубную эмаль и предотвращает развитие кариеса. В десертах ацесульфам К можно применять в качестве единственного подсластителя. В пересчете на сахарозный эквивалент он в 3,6 раза дешевле сахара.
Доказано, что ацесульфам К является нетоксичным веществом — LD501 при пероральном приеме составляет 7,4 г/кг массы тела. Он практически не включается в обменные процессы, не кумулируется, полностью всасывается в кишечнике и быстро выводится почками в неизмененном виде в течение 24 ч (Л.С. Припутина и соавт., 1990; Н.Ю. Тютюнник, 1990), поэтому его употребление рекомендуют ограничивать при сниженной функции почек и заболеваниях, при которых требуется уменьшить потребление калия.
Исследования анальгетического, психотропного, диуретического и бронхолитического действия, а также изучение влияния его на сердечно-сосудистую систему и липидный обмен доказали, что ацесульфам К оказался "инертной субстанцией" в фармакологическом отношении. Длительные и тщательные исследования на экспериментальных животных не выявили мутагенных, канцерогенных, тератогенных и эмбриотоксичес-ких свойств. Кроме того, установлено, что продукты термического распада ацесульфама К (ацетоацетоамид и ацетоацетоа-мид-Ы-сульфоновой кислоты) также не обладают токсическими свойствами (С. Freeze, 1995; М. Wanless, 1996).
На сегодня доказано, что ацесульфам К является идеальным сахарозаменителем для больных сахарным диабетом, ожирением и людей, применяющих диетические продукты, так как не оказывает влияния на уровень глюкозы, инсулина и холестерина крови.
30 июня 1994 г. ацесульфам К был утвержден Европейским парламентом (директива 94/35/ЕС) как сахарозаменитель для употребления в пищу. В 1998 г. FDA разрешило его применение в США в безалкогольных напитках. Научный комитет по пищевым продуктам ЕС определил ежедневную дозу потребления ацесульфама К в 9 мг/кг (март 2000 г.), а Объединенная экспертная комиссии FAO/BO3 по пищевым добавкам и FDA — в 15 мг/кг.
Сукралоза
При изучении сладости различных производных сахарозы в 1976 г. было установлено, что более выраженным сладким вкусом обладает одно из хлорированных производных, которому в дальнейшем присвоили название сукралоза. Получают ее путем замены трех гидроксильных групп в сахарозе на хлор (J. Knight, 1994; S. Wiet, P. Beyts, 1992). При этом интенсивность сладкого вкуса становится в 600 раз выше исходного продукта.
В промышленных масштабах этот сахарозаменитель выпускается под названием "спленда". Он хорошо растворяется в воде, стабилен к температуре при изготовлении пищи и напитков. Применяется в виде таблеток или порошка вместо сахара, используется для приготовления напитков, сладостей, молочных продуктов, различных сухих растворимых смесей.
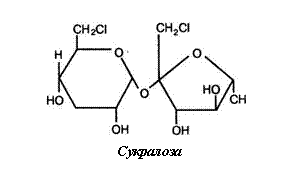 Сукралоза не обладает энергетической ценностью, так как не метаболизируется в организме. Она может использоваться всеми людьми, включая беременных, кормящих женщин и детей любого возраста. Этот сахарозаменитель не влияет на уровень глюкозы и инсулина крови, так как не расщепляется в организме, в отличие от сахарозы, поэтому может без опасений применяться при сахарном диабете (N. Mezitis и соавт., 1994,1997).
Сукралоза не обладает энергетической ценностью, так как не метаболизируется в организме. Она может использоваться всеми людьми, включая беременных, кормящих женщин и детей любого возраста. Этот сахарозаменитель не влияет на уровень глюкозы и инсулина крови, так как не расщепляется в организме, в отличие от сахарозы, поэтому может без опасений применяться при сахарном диабете (N. Mezitis и соавт., 1994,1997).
Изучение влияния сукралозы на различные физиологические показатели у экспериментальных животных и людей (более 100 исследований на протяжении 20 лет) продемонстрировали ее безопасность и безвредность. Доказано, что сукралоза не оказывает повреждающего действия на эмаль зубов, не вызывает генетических и иммунологических повреждений, не обладает канцерогенными и тератогенными свойствами.
Впервые разрешение на ее применение выдано в 1991 г. правительством Канады. В 1999 г. FDA после тщательного изучения разрешила использование этого сахарозаменителя как пищевой добавки в различных продуктах питания без ограничений. Научный комитет по пищевым добавкам ЕС также утвердил положение о применении сукралозы в питании людей (директива 94/35/ЕС). Согласно рекомендациям Объединенного экспертного совета по пищевым продуктам и Объединенного комитета по пищевым добавкам FAO/BO3, ежедневная доза потребления сукралозы не должна превышать 15 мг/кг массы тела.
Дульцин
В 1883 г. было описано получение вещества, обладающего сладким вкусом и имеющим химическое название 4-этоксифе-нилмочевина. В дальнейшем оно получило название дульцин, или сукрол. По своему вкусу это вещество в 150-200 раз слаще сахарозы.
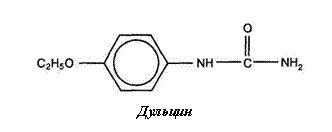 Дульцин использовался для подслащивания напитков в сочетании с сахарином или сахаром. Однако при экспериментальном изучении его безвредности было установлено, что он обладает канцерогенными свойствами и вызывает развитие цирроза печени у крыс. Длительный прием его сопровождался анемией, задержкой роста и повышением смертности (R. Tanaka, 1964; P. Fabiani, 1981). В связи с этим его применение запрещено.
Дульцин использовался для подслащивания напитков в сочетании с сахарином или сахаром. Однако при экспериментальном изучении его безвредности было установлено, что он обладает канцерогенными свойствами и вызывает развитие цирроза печени у крыс. Длительный прием его сопровождался анемией, задержкой роста и повышением смертности (R. Tanaka, 1964; P. Fabiani, 1981). В связи с этим его применение запрещено.
Известно также вещество филодульцин, которое было выделено в 1916 г. из листьев чая Hydrangea macrophylla путем экстракции этиловым спиртом. Это вещество относится к изо-кумаринам и имеет сладкий вкус, в 200-300 раз превосходящий вкус сахарозы. Филодульцин не нашел практического применения.
Таблица перерасчета гликемии, мг% на ммоль/л
| мг% |
ммоль/л |
мг% |
ммоль/л |
мг% |
ммоль/л |
мг% |
ммоль/л |
| 1 |
0,06 |
62 |
3,4 |
115 |
6,4 |
168 |
9,3 |
| 5 |
0,28 |
64 |
3,6 |
116 |
6,4 |
170 |
9,4 |
| 10 |
0,55 |
65 |
3,6 |
118 |
6,5 |
172 |
9,5 |
| 12 |
0,67 |
66 |
3,7 |
120 |
6,7 |
174 |
9,7 |
| 14 |
0,78 |
68 |
3,8 |
122 |
6,8 |
175 |
9,7 |
| 16 |
0,89 |
70 |
3,9 |
124 |
6,9 |
176 |
9,8 |
| 18 |
1,0 |
72 |
4,0 |
125 |
6,9 |
178 |
9,9 |
| 20 |
1,1 |
74 |
4,1 |
126 |
7,0 |
180 |
10,0 |
| 22 |
1,2 |
75 |
4,2 |
128 |
7,1 |
182 |
10,1 |
| 24 |
1,3 |
76 |
4,2 |
130 |
7,2 |
184 |
10,2 |
| 25 |
1,4 |
78 |
4,3 |
132 |
7,3 |
185 |
10,3 |
| 26 |
1,4 |
80 |
4,4 |
134 |
7,4 |
186 |
10,3 |
| 28 |
1,6 |
82 |
4,6 |
135 |
7,5 |
188 |
10,4 |
| 30 |
1,7 |
84 |
4,7 |
136 |
7,5 |
190 |
10,5 |
| 32 |
1,8 |
85 |
4,7 |
138 |
7,7 |
192 |
10,7 |
| 34 |
1,9 |
86 |
4,8 |
140 |
7,8 |
194 |
10,8 |
| 35 |
1,9 |
88 |
4,9 |
142 |
7,9 |
195 |
10,8 |
| 36 |
2,0 |
90 |
5,0 |
144 |
8,0 |
196 |
10,9 |
| 38 |
2,1 |
92 |
5,1 |
145 |
8,0 |
198 |
11,0 |
| 40 |
2,2 |
94 |
5,2 |
146 |
8,1 |
200 |
11,1 |
| 42 |
2,3 |
95 |
5,3 |
148 |
8,2 |
225 |
12,5 |
| 44 |
2,4 |
96 |
5,3 |
150 |
8,3 |
250 |
13,9 |
| 45 |
2,5 |
98 |
5,4 |
152 |
8,4 |
275 |
15,3 |
| 46 |
2,6 |
100 |
5,5 |
154 |
8,5 |
300 |
16,6 |
| 48 |
2,7 |
102 |
5,7 |
155 |
8,6 |
325 |
18,0 |
| 50 |
2,8 |
104 |
5,8 |
156 |
8,7 |
350 |
19,4 |
| 52 |
2,9 |
105 |
5,8 |
158 |
8,8 |
375 |
20,8 |
| 54 |
3,0 |
106 |
5,9 |
160 |
8,9 |
400 |
22,2 |
| 55 |
3,1 |
108 |
6,0 |
162 |
9,0 |
425 |
23,6 |
| 56 |
3,1 |
110 |
6,1 |
164 |
9,1 |
450 |
25,0 |
| 58 |
3,2 |
112 |
6,2 |
165 |
9,2 |
475 |
26,4 |
| 60 |
3,3 |
114 |
6,3 |
166 |
9,2 |
500 |
27,7 |
Примечание: 18,016 х ммоль/л = мг%; 0,0555 х мг% = ммоль/л.
Коды некоторых пищевых добавок, принятые в ЕС
| Е412 |
Гуаровая смола |
| Е414 |
Гуммиарабик (смолаакации) |
| Е420 |
сорбит |
| Е421 |
маннит |
| Е422 |
глицерин |
| Е440 |
пектины |
| Е460 |
целлюлоза |
| Е461 |
метилцеллюлоза |
| Е463 |
гидроксипропилцеллюлоза |
| Е464 |
гидроксиметилцеллюлоза |
| Е466 |
карбоксиметилцеллюлоза |
| Е636 |
мальтол |
| Е950 |
Ацесульфам К |
| Е951 |
аспартам |
| Е952 |
цикламатнатрия |
| Е953 |
изомальт |
| Е954 |
сахарин |
| Е957 |
Тауматин (толькокакусилительаромата) |
| Е959 |
неогесперединDC |
| Е965 |
мальтитол |
| Е966 |
лактол |
| Е967 |
ксилит |